
跨膜蛋白裝配γ-分泌酶是約100種1型跨膜蛋白的受調控膜內加工(RIP)中的關鍵蛋白酶。 重要的是,它在 阿爾茨海默病 (AD)中具有病理作用,因為它從淀粉樣前體蛋白(APP)生成神經毒性淀粉樣β肽。因此,從生物學和治療學的角度來看, γ-分泌酶的定位研究 都是至關重要的。
盡管在許多實驗室中進行了幾年的努力,目前尚不清楚γ-分泌酶在神經元中的何處發揮其活性。其中技術挑戰之一是,活性酶含有四種蛋白質組分,并且大多數亞細胞區室不能通過傳統光學顯微鏡進行空間分辨。
研究介紹(節選)
γ-分泌酶是阿爾茨海默病(AD)病理學中的關鍵角色,因為它催化淀粉樣前體蛋白(APP)加工的最后一步,導致神經毒性淀粉樣β-肽(Aβ)的形成,Aβ是AD患者大腦中淀粉樣斑塊的主要成分。γ-分泌酶產生長度可變的Aβ,尤其是42和43個氨基酸的變體(Aβ42和Aβ43)易于形成神經毒性寡聚體。AD患者海馬神經元中Aβ42的細胞內水平升高,在突觸中蓄積,并與AD病理學相關。直接抑制γ-分泌酶作為AD的治療策略是復雜的,因為除APP外,該酶還有大約100種不同的底物,包括Notch。重要的是,已證明Aβ是在突觸處產生的,這是在突觸前還是突觸后發生的還存在爭議。這種不確定性部分是由于確定突觸亞結構所涉及的技術挑戰。
在這里,作者使用了兩種納米技術 STORM 和 STED 顯微鏡的強大組合來可視化γ-分泌酶在神經元中的位置。作者發現γ-分泌酶存在于 突觸前 和 突觸后區室 。研究中,作者進一步表明該酶在 突觸后膜中 非常接近突觸間隙處富集,以及NMDA受體表明γ-分泌酶存在于突觸后質膜。研究中,作者以高精度的數據顯示了 突觸的三維位置 ,并解決了長期以來關于γ-分泌酶突觸位置的爭論。
研究結果(節選)
共聚焦顯微鏡顯示,樹突形成了幾個突觸,軸突與樹突平行或在樹突之間延伸(圖1a),在軸突和樹突中都發現了γ-分泌酶,并在突觸中富集(圖1a)。PS1和nicastrin的染色顯示,這些成分與GTB在相同的區域,也在其他區域發現(圖1b和c)。在單獨生長的軸突中,即在很大程度上與樹突分離的軸突中,γ-分泌酶富集在前扣突結構中(圖1d)。這種酶也在軸突末端突觸中富集(圖1d)。γ-分泌酶的STED圖像,與作為軸突標記物的Tau蛋白共同標記,進一步證實γ-分泌酶在前結中富集,并且顯示γ-分泌酶染色在前結的外部最強(圖1e)。通過STORM圖像進一步證實了γ-分泌酶在棘上的富集,其中γ-分泌酶被GTB和Alexa 647標記的鏈霉親和素染色(圖1f)。因此,三種不同的顯微鏡技術顯示γ-分泌酶在神經元突觸處富集。
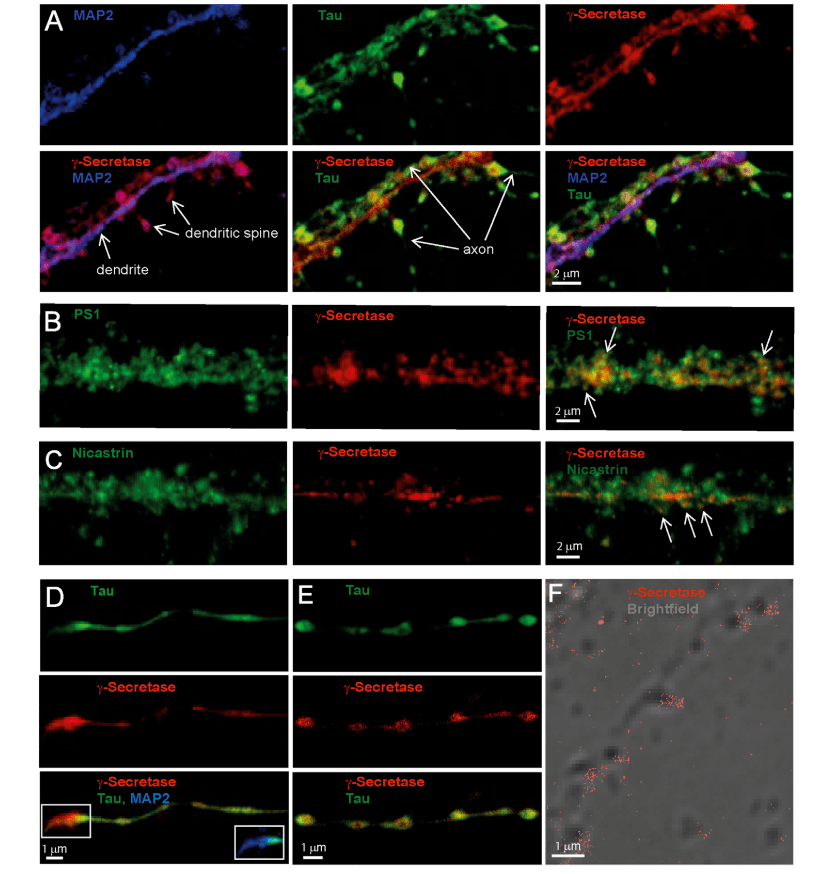 圖1 通過 dSTORM等 分析小鼠原代海馬神經元軸突、樹突和棘中γ-分泌酶的定位。
圖1 通過 dSTORM等 分析小鼠原代海馬神經元軸突、樹突和棘中γ-分泌酶的定位。
(a)MAP 2染色(藍色)、tau(綠色)和γ-分泌酶(紅色)染色的周圍軸突的放大樹突的共焦圖像。如圖所示,在上部面板中顯示各個污漬,而在下部面板中顯示合并圖像的不同組合。(b)樹突特寫中PS1和γ-分泌酶標記的共聚焦圖像。箭頭指向PS1和γ-分泌酶共染色的突觸區域(黃色)。(c)樹突特寫中PS1和nicastrin標記的共聚焦圖像。箭頭指向突觸區,同時染色的是nicastrin和γ-分泌酶(黃色)。(d)共焦圖像相同的細胞的軸突與τ(a)染色在綠色上面板,γ-secretase紅色中間面板和合并后的圖像在底部面板。合并后的形象的插圖顯示了一個放大部分的MAP2(藍色)。(e)結合共聚焦顯微鏡和STED顯微鏡(γ-分泌酶,中圖)觀察軸突結中活性γ-分泌酶的富集。底部面板中顯示合并圖像。(f)活性γ-分泌酶(紅色)的dSTORM圖像與明場圖像重疊。注意棘上活性γ-分泌酶的富集。
γ-分泌酶在突觸處的富集使我們研究該酶是否存在于突觸前或突觸后區室中,這些區室由僅20-25nm寬的裂隙隔開。這個距離比傳統共聚焦顯微鏡獲得的分辨率小10倍左右,因此STORM被用于更好地顯示突觸位置。由于我們用STORM進行成像,因此我們可以從不同角度研究突觸素和γ-分泌酶的分布(圖2a)。γ-分泌酶和突觸囊泡蛋白之間的接近度從各個角度都很明顯,在某些情況下,突觸囊泡蛋白和γ-分泌酶信號之間的距離小于10nm。
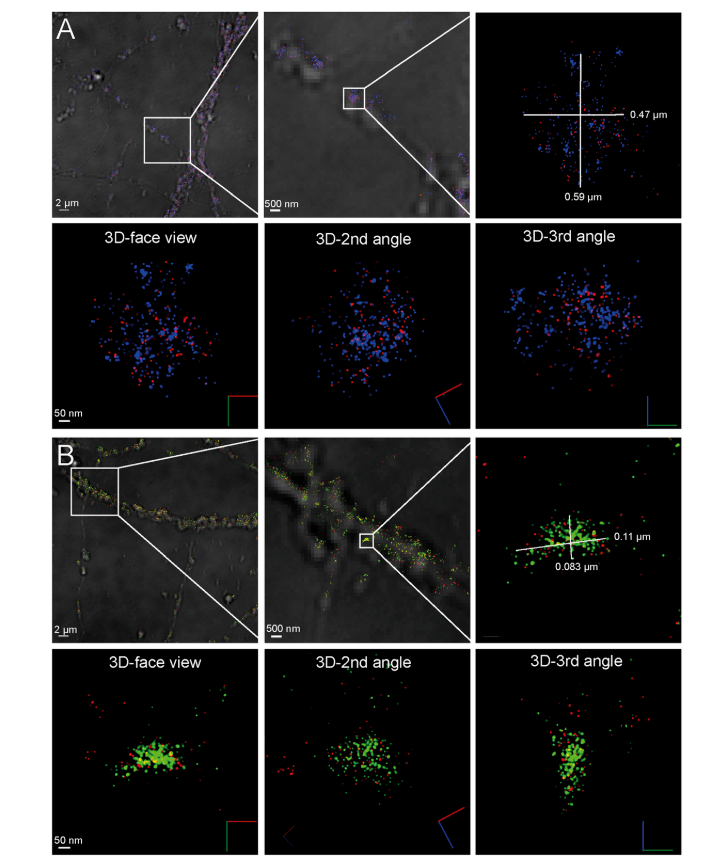 圖2 突觸中γ-分泌酶的STORM成像
圖2 突觸中γ-分泌酶的STORM成像
(a)活性γ-分泌酶在突觸前區的定位顯示γ-分泌酶(紅色)和突觸前標記突觸囊泡蛋白(藍色)。左上方的面板顯示了典型的STORM圖像,左側為明場疊加,中間和右側面板放大,右側顯示了單個突觸區域。下圖從三個不同角度顯示了在3D視圖中顯示的相同突觸,其中紅色、綠色和藍色線分別表示X、Y和Z方向。(b)活性γ-分泌酶在突觸后區的定位,顯示γ-分泌酶(紅色)和突觸后標記物PSD 95(藍色)。左上方的面板顯示了典型的STORM圖像,位于左側的明場覆蓋圖上,中間和右側面板的放大倍數增加。下面板從三個不同角度顯示了3D視圖中顯示的同一突觸,其中符號中的紅色、綠色和藍色線分別表示X、Y和Z方向。
突觸后密度和突觸間隙之間的距離表明γ-分泌酶在突觸后質膜中富集(圖5a-e)。STORM分析顯示NMDAR2B和γ-分泌酶之間非常接近,這為突觸后膜中存在γ-分泌酶提供了進一步的證據(圖3)。
 圖3 γ-分泌酶在突觸后質膜的定位
圖3 γ-分泌酶在突觸后質膜的定位
(a)STED圖像顯示γ-分泌酶(紅色)非常靠近樹突棘中的突觸間隙(白色箭頭)。突觸素(藍色)和PSD95(綠色)分別標記突觸前和突觸后側。(b)γ-分泌酶(紅色)和NMDAR 2B(綠色)的STORM成像。(c)與(b)中的右圖相同的突觸后膜區域從三個不同角度顯示在3D視圖中,其中紅色、綠色和藍色線分別表示X、Y和Z方向。
通過以上研究結果,作者發現γ-分泌酶主要存在于突觸前區室的細胞內細胞器中,而在突觸后區室的細胞內細胞器和質膜中都有發現。突觸前和突觸后區室中的豐度隨著突觸的成熟而增加。作者的研究結果表明,Aβ可以在突觸前和突觸后區室產生。因此,本研究對于進一步了解AD病理學具有重要意義,這與未來創建開發AD治療的新方法密切相關。
iSTORM預約試拍
目前在國內,隨機光學重建顯微鏡STORM已成功實現商用,有需要STORM成像技術進行實驗研究的專家老師們,請文末填寫問卷,即可預約獲得 iSTORM 超高分辨率顯微成像系統試拍服務~
力顯智能現已發布的超高分辨率顯微成像系統 iSTORM,成功實現了光學顯微鏡對衍射極限的突破,使得在20納米的分辨率尺度上從事生物大分子的單分子定位與計數、亞細胞及大分子復合物結構解析、生物大分子生物動力學等的研究成為現實,從而給生命科學、醫學等領域帶來重大突破 。

雙12特惠??iSTORM免費試拍:每個課題組都有1次免費試拍機會,需要用戶提供樣本和一抗,需提前溝通。
超高分辨率顯微成像系統iSTORM具有20nm超高分辨率、 3D成像、多通道同時成像光路設計、實時重構、2小時新手掌握等特點,已實現活細胞單分子定位與計數,并提供熒光染料選擇、樣本制備、成像服務與實驗方案整體解決方案,以納米級觀測精度、高穩定性、廣泛環境適用、快速成像、簡易操作等優異特性,獲得了超過50家科研小組和100多位科研人員的高度認可。
參考文獻
References
[1] G. Mitchell, R. R. Isberg, Cell Host Microbe 2017, 22,166–175.
[2] S. Pandey, T. Kawai, S. Akira, Cold Spring Harbor Perspect. Biol. 2015, 7,a016246.
[3] a) M. S. Siegrist, S. Whiteside, J. C. Jewett, A. Aditham,F.Cava, C. R. Ber-tozzi, ACS Chem. Biol. 2013, 8,500–505;b)P.Shieh,M.S.Siegrist, A. J.Cullen, C. R. Bertozzi, Proc. Natl. Acad. Sci. USA 2014, 111,5456–5461;c) G. W. Liechti, E. Kuru, E. Hall, A. Kalinda,Y.V.Brun, M. VanNieuwenhze,A. T. Maurelli, Nature 2014, 506,507–510.
[4] a) B. M. Swarts, C. M. Holsclaw, J. C. Jewett, M. Alber,D.M.Fox, M. S.Siegrist, J. A. Leary,R.Kalscheuer,C.R.Bertozzi,J.Am.Chem.Soc.2012,134,16123–16126; b) K. M.Backus,H.I.Boshoff, C. S. Barry,O.Boutur-eira, M. K. Patel, F. D’Hooge, S. S. Lee, L. E. Via, K. Tahlan, C. E. Barry,B.G.Davis, Nat. Chem.Biol. 2011, 7,228–235;c)F.P.Rodriguez-Rivera, X.Zhou, J. A. Theriot, C. R. Bertozzi, J. Am. Chem. Soc. 2017, 139,3488–3495.
[5] D. C. Dieterich, A. J. Link, J. Graumann, D. A. Tirrell, E. M. Schuman, Proc.
Natl. Acad. Sci. USA 2006, 103,9482–9487.
[6] A.Mahdavi,J.Szychowski,S.Hess, O. Schneewind,S.K.Mazmanian, D. A. Tirrell, Proc. Natl. Acad. Sci.USA 2014, 111,433–438.
[7] a) M. Grammel, P. D. Dossa, E. Taylor-Salmon,H.C.Hang, Chem.Commun. 2012, 48,1473–1474;b)M.Grammel, M. M. Zhang, H. C.Hang, Angew.Chem. Int. Ed. 2010, 49,5970–5974; Angew.Chem. 2010,122,6106–6110; c) S. Lin, Z. Zhang, H. Xu, L. Li, S. Chen, J. Li, Z. Hao,P. R. Chen, J. Am. Chem. Soc. 2011, 133,20581–20587.
[8] J. T. Ngo, J. A. Champion, A. Mahdavi, I. C. Tanrikulu, K. E. Beatty, R. E.Connor,T.H.Yoo, D. C.Dieterich, E. M. Schuman, D. A. Tirrell, Nat. Chem.Biol. 2009, 5,715–717.
[9] A. G. Chande, Z. Siddiqui,M.K.Midha, V. Sirohi, S. Ravichandran, K. V. S.Rao, Sci. Rep. 2015, 5,13430.
[10] R. Hatzenpichler,S.A.Connon, D. Goudeau, R. R. Malmstrom,T.Woyke,V. J. Orphan, Proc. Natl. Acad. Sci. USA 2016, 113,E4069–E4078.



