隨機光學重建顯微鏡(stochastic optical reconstruction microscopy,簡稱STORM),是一種超分辨率顯微鏡,其分辨率比傳統(tǒng)光學顯微鏡高10倍以上。
我們知道,光學顯微鏡憑借其非接觸、無損傷等優(yōu)點,長期以來是生物醫(yī)學研究的重要工具。但由于光的衍射限制了光學顯微鏡的分辨率,傳統(tǒng)的顯微鏡已經不適于生命科學研究中的超微結構成像了。本文將從原理、應用等方面對隨機光學重建顯微鏡STORM進行相關研究,若表述不正確或者不到位,請各位老師指正。
01光的衍射限制了光學顯微鏡的分辨率
在了解STORM之前,需要先知悉一個概念。眾所周知,光學顯微鏡是用可見光來觀察生物樣品的。而光是一種橫波,當它經過一個圓孔,且這個圓孔的大小與光的波長差別不大時,光在此時不會沿直線傳播,而是在各個方向上“溜走”。 光在傳播過程中,遇到障礙物或小孔時,光將偏離直線傳播的路徑而繞到障礙物后面?zhèn)鞑サ默F(xiàn)象,這就叫 光的衍射 。
由此而形成的圓孔衍射圖樣,叫“艾里斑”(圖1)。正因如此,任何一種顯微鏡系統(tǒng)都無法把光線在像平面匯聚成無限小的點,而是只能形成有限大小的艾里斑。如果兩個點很接近,像平面上的兩個艾里斑就幾乎重合在一起,那物平面上的兩個點就不可分辨了。

圖1、“艾里斑”概念圖
所以,光的衍射使得光學顯微鏡的分辨率存在著極限(約為200 nm),使得傳統(tǒng)顯微鏡無法清晰觀察尺寸在200 nm以內的生物結構,極大制約了生命科學研究的發(fā)展。
02超分辨率顯微鏡打破分辨率極限
科研工作者為了看到更精細的生命體精細結構,就要想辦法突破這一成像障礙。為此,多種超分辨率顯微鏡被開發(fā)了出來(超越了光學顯微鏡的分辨率極限,故被稱為超分辨顯微鏡)。 在這里,我們集中討論其中這樣一個具有相對優(yōu)勢的顯微鏡: 隨機光學重建顯微鏡STORM 。
在2006年的Nature上,莊小威與其它同事發(fā)現(xiàn)了一種能夠數(shù)百次反復在各種顏色的光照下使用且可在熒光態(tài)和暗態(tài)轉化的發(fā)光分子團,從而得到了一種比傳統(tǒng)光學顯微鏡高10倍以上分辨率的顯微技術,并將其命名為隨機光學重建顯微鏡,簡稱STORM。
03隨機光學重建顯微鏡STORM技術原理簡介
正如前面提到的那樣,兩個挨得很近的光點會讓我們分辨不出誰是誰,那么如果我們分開來看呢?
也就是說,當我們照射并觀察第一個點時,第二個點并不會發(fā)光,自然不會產生艾里斑影響我們觀察第一個點,前者艾里斑的中心點位置就是熒光分子的準確位置。 接下來,通過某種方法,讓第二個點被照亮。這個時候第一個點又不在光斑的照明范圍之內了,同樣不會干擾對第二個點的觀察。通過這種“以時間換空間”的設計,巧妙地繞開了阿貝極限(顯微鏡分辨極限)的束縛,將光學顯微鏡的分辨率大大提高。
STORM技術就運用了這種思想,它使用的是有機熒光分子對染料,并且通過一些方法使細胞內的一小部分熒光分子發(fā)光,而不是全部。這樣由于發(fā)光的點分布比較分散,重疊比較少,因此每個光暈可以近似為一個熒光分子。在一次激發(fā)中,可以確定一部分光暈的中心,在下一次激發(fā)中,可以確定另外一部分光暈的中心,把這許多次激發(fā)的結果疊加,就是完整而清晰的圖像。
STROM成像過程包含一系列圖像循環(huán)。每個循環(huán)中,只打開視野下一部分熒光基團,這樣每個活躍的熒光集團都被分辨,它們的圖像與其他分子分開,不重疊。這樣確定了基團的準確位置,多次重復這個過程,每次隨機打開熒光基團的不同亞基,得到圖像,確定每個亞基的位置后,把以上圖像重建成清晰的整個圖像。 理論上STORM可得到分辨率達到幾個納米的熒光圖像。
04隨機光學重建顯微鏡STORM技術應用案例
隨機光學重建顯微鏡(STORM)是一種超分辨率顯微技術,能夠在二維或三維、多種顏色下成像,甚至可以對活細胞成像。這種成像技術的方法根據(jù)正在成像的內容、如何成像以及正在產生的圖像類型而變化很大,可以應用于生命科學的許多領域,并為從神經科學到亞細胞科學的許多不同需求提供非常高分辨率的圖像。自STORM技術被提起以來,越來越多的研究人員認識到了這項技術的優(yōu)勢并廣泛運用于研究中。
(以近些年的部分研究成果為例)
2013年,cell 雜志上的一篇研究報告:莊小威團隊利用超分辨率熒光成像方法(STORM)對端粒 DNA 進行原位成像,直接可視化染色質中的 T 環(huán)結構,并系統(tǒng)地評估保護蛋白在 T 環(huán)形成中的作用。
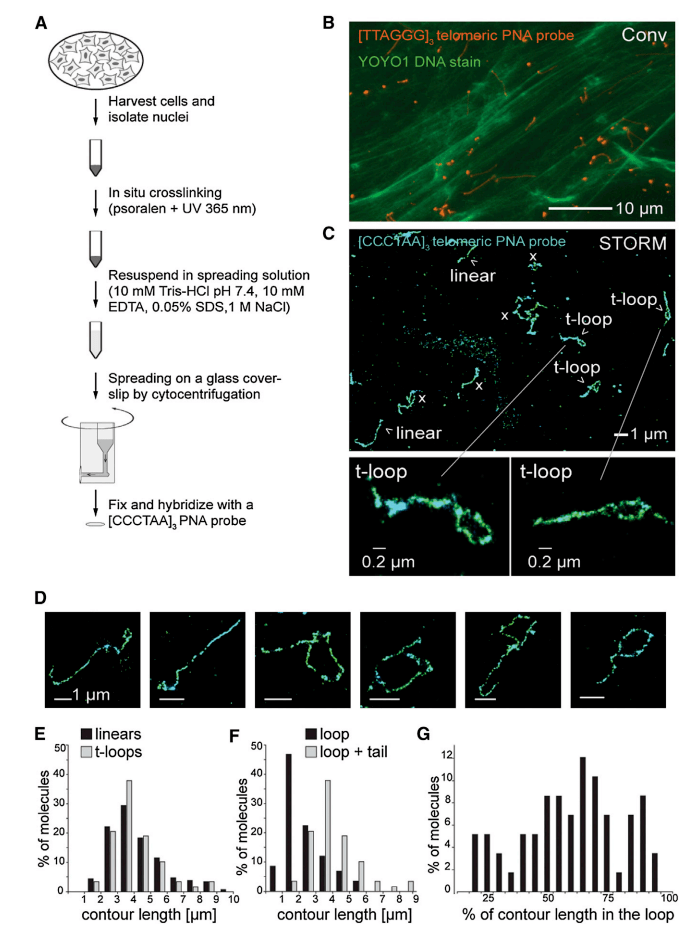
圖3、STORM 成像顯示染色質擴散后的 T 環(huán)
2017年,Liu Riyue團隊開發(fā)了一種光漂白的方法,以有效地降低藍藻和植物細胞的自身熒光并利用STORM技術在球形藍藻原綠球菌和開花植物擬南芥中獲得了~10nm的橫向分辨率。
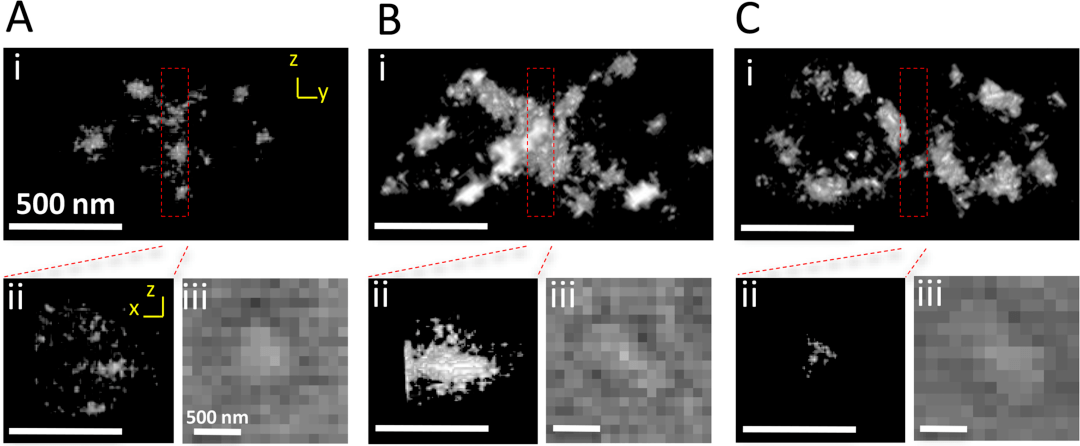
圖4、雙Z環(huán)的STORM圖像
2018年,Lin, Danying團隊提出了一種在固定樣本上采用Refresh熒光探針的方法,擴展了多層 3D STORM的成像深度,并顯示了COS-7 細胞中微管、線粒體和內質網(wǎng)的三通道、擴展深度 3D prSTORM圖像。
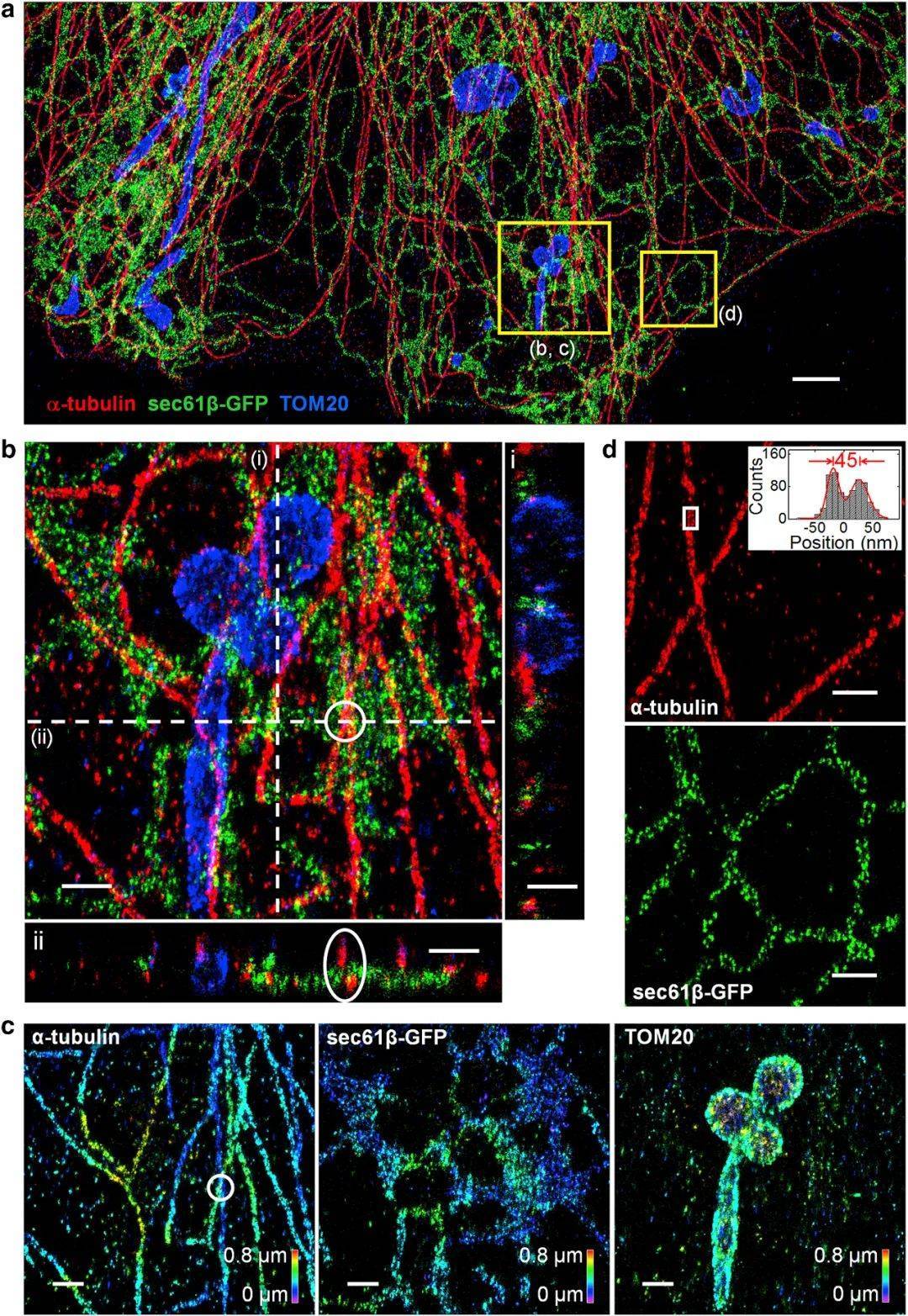
圖5、 COS-7 細胞中微管、線粒體和內質網(wǎng)的三通道、擴展深度 3D prSTORM 圖像
2019,Schlegel J , Peters S , Doose S 團隊通過直接隨機光學重建顯微鏡(dSTORM)進行超分辨率顯微鏡觀察,顯示腦膜炎球菌周圍有GM1聚集,突出了其對細菌侵襲的重要意義。
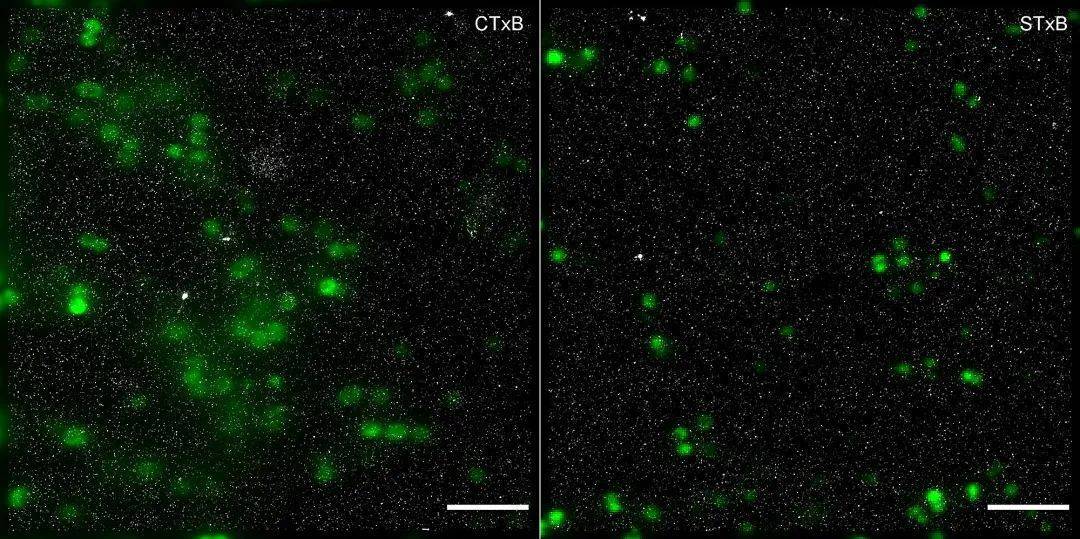
圖6、表達GFP的腦膜炎球菌(綠色)的GM1和Gb3的dSTORM圖像
2021,Hazime, K.S., Zhou, Z., Joachimiak團隊運用STORM技術發(fā)現(xiàn),表達IFT融合蛋白的細胞在纖毛基部,IFT亞基位于九個不同的位點,在它們進入纖毛干之前,IFT蛋白以高親和力停靠在纖毛基部的9個位點。
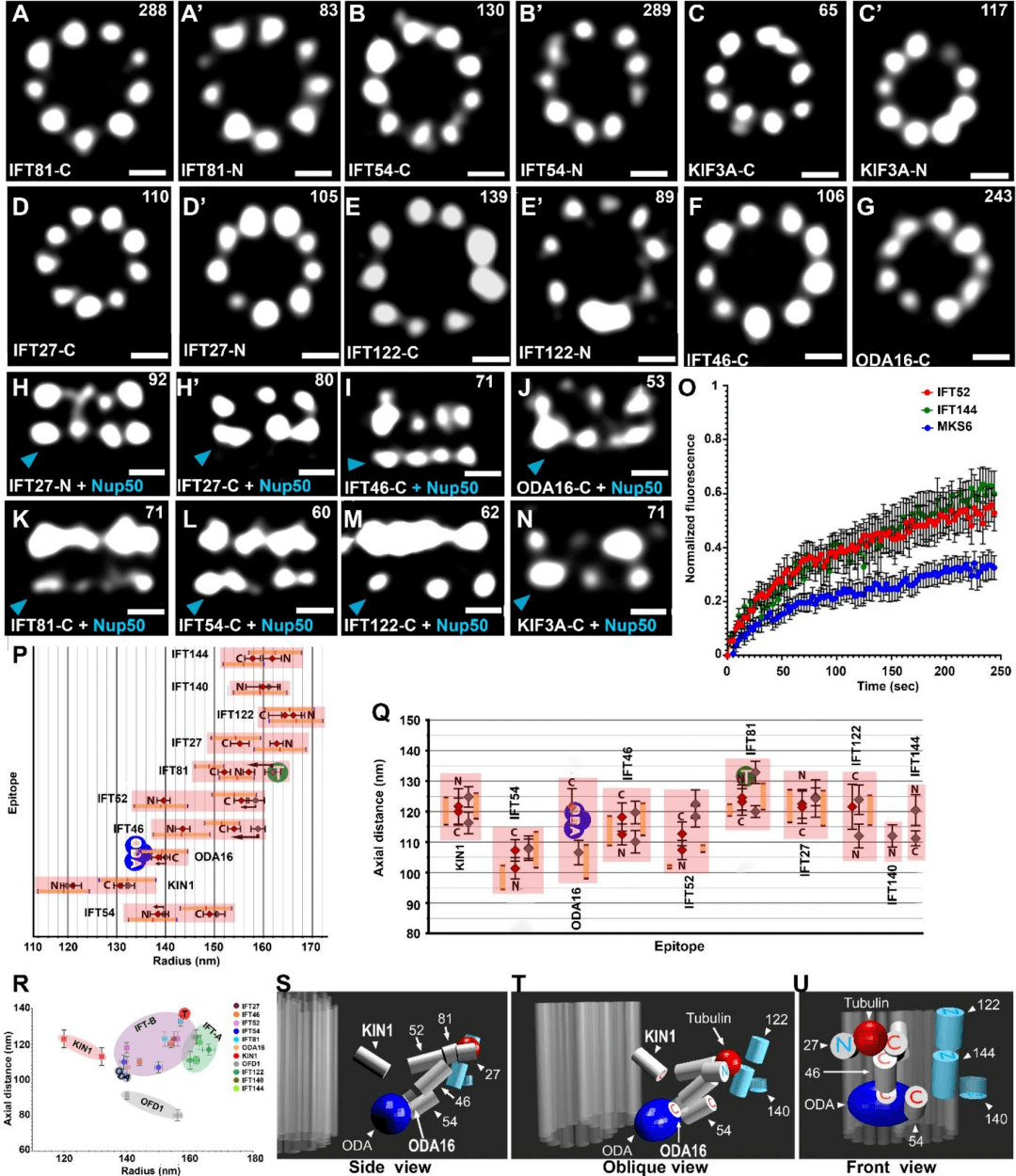
圖7、IFT顆粒蛋白的定位,N-或C-末端3HA標記的IFT蛋白、KIN1/KIF3A驅動蛋白和銜接蛋白ODA16的頂視圖和側(側)視圖的STORM圖像。
2021,Blandin, Anne-Florence團隊利用球狀體膠質瘤細胞擴散的體外模型,發(fā)現(xiàn)α5整合素缺失的細胞比表達α5的細胞對TKIs更敏感。
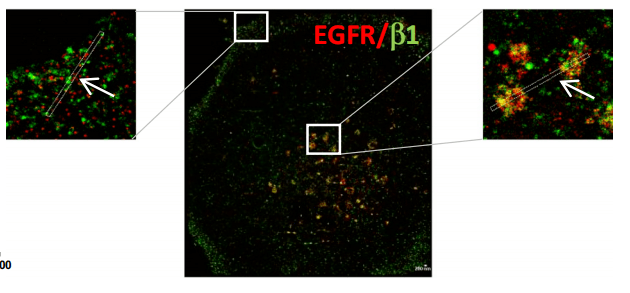
圖8、吉非替尼處理的細胞的雙色dSTORM圖像顯示細胞外周和核內體上的EGFR/β1整合素復合體
STORM因為其優(yōu)異的單分子成像能力,越來越多的被用在細胞精細結構的探索。對STORM的更多研究將提供更有效的方法來制備樣品和成像樣品,以及提供更高分辨率的圖像。相信在未來這項技術能得到進一步發(fā)展,變成功能更為強大的利器。
05超高分辨顯微成像系統(tǒng)iSTORM
現(xiàn)已發(fā)布的超高分辨率顯微成像系統(tǒng) iSTORM,成功實現(xiàn)了光學顯微鏡對衍射極限的突破,使得在 20 nm的分辨率尺度上從事生物大分子的單分子定位與計數(shù)、亞細胞及超分子結構解析、生物大分子生物動力學等的研究成為現(xiàn)實,從而給生命科學、醫(yī)學等領域帶來重大突破 。

超高分辨率顯微成像系統(tǒng) iSTORM 具有 20 nm超高分辨率、3通道同時成像、3D同步拍攝、實時重構、2小時新手掌握 等特點,已實現(xiàn)活細胞單分子定位與計數(shù),并提供熒光染料選擇、樣本制備、成像服務與實驗方案整體解決方案, 以納米級觀測精度、高穩(wěn)定性、廣泛環(huán)境適用、快速成像、簡易操作等優(yōu)異特性,獲得了高度認可。
參考文獻:
1、Rust M J, Bates M, Zhuang X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM)[J]. Nature methods, 2006, 3(10): 793-796.
2、Doksani Y, Wu JY, de Lange T, Zhuang X. Super-resolution fluorescence imaging of telomeres reveals TRF2-dependent T-loop formation. Cell. 2013 Oct 10;155(2):345-356. doi: 10.1016/j.cell.2013.09.048. PMID: 24120135; PMCID: PMC4062873.
3、Liu, Riyue, et al. "Three-dimensional superresolution imaging of the FtsZ ring during cell division of the cyanobacterium Prochlorococcus." MBio 8.6 (2017): e00657-17.
4、Lin, Danying, et al. "Extended-depth 3D super-resolution imaging using Probe-Refresh STORM." Biophysical journal 114.8 (2018): 1980-1987.
5、Schlegel J , Peters S , Doose S , et al. Super-Resolution Microscopy Reveals Local Accumulation of Plasma Membrane Gangliosides at Neisseria meningitidis Invasion Sites[J]. Frontiers in Cell and Developmental Biology, 2019, 7.
6、Hazime, K.S., Zhou, Z., Joachimiak, E. et al. STORM imaging reveals the spatial arrangement of transition zone components and IFT particles at the ciliary base in Tetrahymena. Sci Rep 11, 7899 (2021).
7、Blandin, Anne-Florence, et al. "Gefitinib induces EGFR and α5β1 integrin co-endocytosis in glioblastoma cells." Cellular and Molecular Life Sciences 78.6 (2021): 2949-2962.



