

01研究背景
超分辨率顯微鏡技術(shù)提供了亞衍射極限的分辨率,與傳統(tǒng)的共焦顯微鏡相比,分辨率提高了2到10倍。光學(xué)顯微鏡分辨率的這一突破為神經(jīng)科學(xué)和突觸生物學(xué)的新發(fā)現(xiàn)做出了貢獻(xiàn)。本文綜述了結(jié)構(gòu)照明顯微鏡(SIM)、受激發(fā)射損耗顯微鏡(STED)和隨機(jī)光學(xué)重構(gòu)顯微鏡(STORM)/單分子定位顯微鏡(SMLM)技術(shù),并對(duì)它們進(jìn)行了比較,以更好地理解它們之間的差異及其在突觸生物學(xué)分析中的適用性。本文還就這些顯微技術(shù)的實(shí)用層面進(jìn)行了討論,包括分辨率、圖像采集速度、多色能力及其他優(yōu)缺點(diǎn)。此外,本文還總結(jié)了超分辨率顯微鏡如何用于分析神經(jīng)肌肉接頭和突觸的方法。
神經(jīng)肌肉接頭 (NMJ) 是在運(yùn)動(dòng)神經(jīng)元和肌肉纖維之間形成的大型突觸。由于它們的大尺寸和可訪(fǎng)問(wèn)性,這些突觸已經(jīng)被研究人員們使用組織學(xué)和生理學(xué)的方法進(jìn)行了非常廣泛的研究。即使針對(duì)這些突觸的研究歷史已經(jīng)非常悠久了,但近來(lái)超分辨率顯微鏡的出現(xiàn)和投入使用,還是使得這類(lèi)研究有了新的發(fā)現(xiàn)。
02研究介紹(節(jié)選)
一、SIM、STED 和 STORM 超分辨率顯微鏡的優(yōu)缺點(diǎn)
1、分辨率
超分辨率顯微鏡提供亞衍射極限分辨率,優(yōu)于約 200 nm 的共聚焦顯微鏡的分辨率。在神經(jīng)生物學(xué)中,共聚焦顯微鏡可以對(duì)軸突和神經(jīng)、樹(shù)突樹(shù)狀形態(tài)、線(xiàn)粒體形態(tài)、細(xì)胞核、突觸和 NMJ 進(jìn)行成像。然而,超分辨率顯微鏡可用于對(duì)棘的詳細(xì)結(jié)構(gòu)、Ranvier 節(jié)點(diǎn)中的蛋白質(zhì)分布模式、核孔蛋白質(zhì)、突觸前和突觸后蛋白質(zhì)的亞突觸定位以及突觸囊泡進(jìn)行成像。
以NMJ為例,NMJ的正面視圖很大,尺寸范圍約為 10 – 60 μm(人類(lèi)、小鼠); 然而,這種突觸的一些關(guān)鍵特征的尺寸低于 200 nm 的衍射極限分辨率。例如,突觸囊泡為 55 nm,活動(dòng)區(qū)為 50 – 100 nm,突觸間隙為 50 – 100 nm;此外,結(jié)折峰寬度為 207 nm,開(kāi)口寬度為 55 nm (圖1),層粘連蛋白長(zhǎng)度為 77 nm,Lrp4 蛋白長(zhǎng)度約為 60 nm。因此,分析這些特征需要提高超分辨率顯微鏡的分辨率。
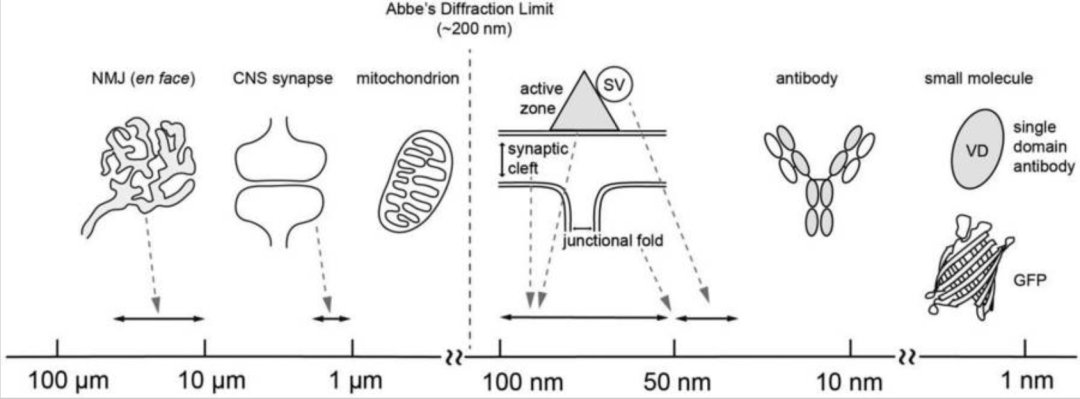
圖1、 阿貝的衍射極限,突觸結(jié)構(gòu)的大小以及用于超分辨率顯微鏡的工具
這三種技術(shù)的 XY 平面分辨率如下:SIM,120 nm,STED 和 STORM,20 – 30 nm (表1)。與共聚焦顯微鏡相比,它們的分辨率顯著提高,共聚焦顯微鏡在 XY 平面上的分辨率約為 200 nm,沿 Z 軸的分辨率約為 500 nm(對(duì)于使用 NA=1.4 透鏡觀(guān)察到的綠色熒光染料)。因?yàn)榻箙^(qū)較寬,共聚焦顯微鏡的 Z 軸分辨率低于 XY 分辨率。超分辨率顯微鏡技術(shù)的 Z 軸分辨率如下:SIM,300 nm,STED,75 – 100 nm(Easy 3D,STED 3×)和 STORM,50 nm(STORM 3D)。
除了分辨率的差異之外,這三種技術(shù)在提高分辨率的機(jī)制上也有所不同。SIM 和 STORM 基于原始數(shù)據(jù)顯微照片的后處理來(lái)重建超分辨率圖像,STED 顯微鏡使用應(yīng)用于原始數(shù)據(jù)顯微照片的傅里葉變換生成超分辨率圖像。STED 顯微鏡通過(guò)在樣品上掃描激光束來(lái)生成超分辨率圖像,類(lèi)似于共聚焦顯微鏡。STORM 通過(guò)收集數(shù)千張顯微照片并使用高斯分布近似和分配點(diǎn)來(lái)重建它們,類(lèi)似于點(diǎn)畫(huà)法,從而生成超分辨率圖像。
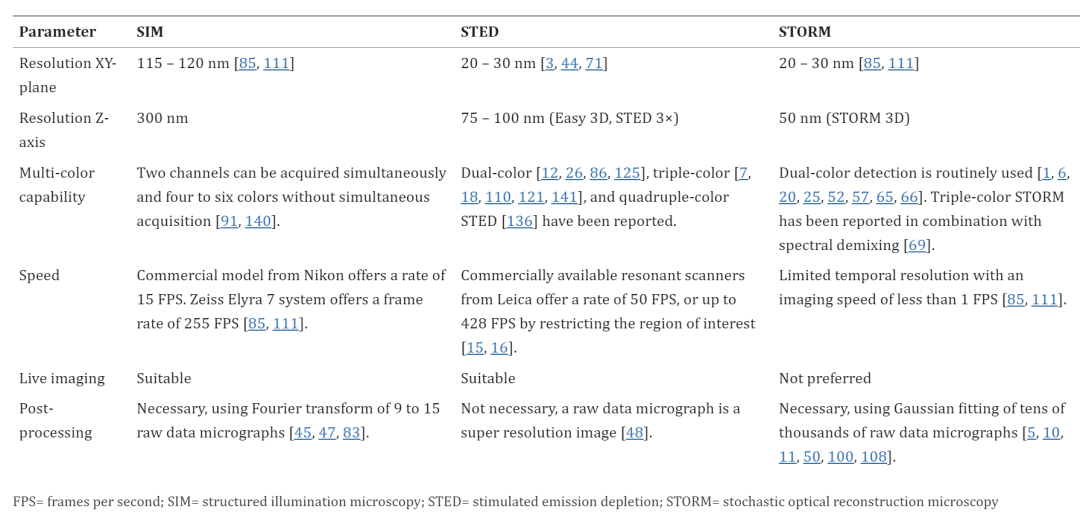
表1、超分辨率顯微鏡規(guī)格比較
2、顏色數(shù)
與傳統(tǒng)的熒光顯微鏡技術(shù)類(lèi)似,超分辨率顯微鏡可以使用多種顏色進(jìn)行。SIM 的圖像構(gòu)建依賴(lài)于對(duì) 9 到 15 個(gè)采集到的具有莫爾條紋的圖像進(jìn)行后處理;因此,如果激發(fā)和發(fā)射波長(zhǎng)在熒光團(tuán)之間分離,則可以進(jìn)行多色成像。
在 STED 顯微鏡中,通過(guò)用激發(fā)激光掃描樣品并獲取每個(gè)熒光團(tuán)的發(fā)射波長(zhǎng)來(lái)生成類(lèi)似于共聚焦顯微鏡的圖像。與共聚焦顯微鏡的區(qū)別在于需要將熒光團(tuán)的發(fā)射波長(zhǎng)與 STED 激光的波長(zhǎng)相匹配,以將激發(fā)的熒光團(tuán)耗盡至基態(tài)。
STORM 需要高強(qiáng)度光下在非發(fā)射狀態(tài)和基態(tài)之間切換的熒光團(tuán),以及用于這些切換熒光團(tuán)的專(zhuān)用緩沖環(huán)境。熒光團(tuán)隨機(jī)弛豫到基態(tài),然后被激發(fā)發(fā)射熒光。具有這些特性的熒光團(tuán)稱(chēng)為光可切換(光閃爍)染料(對(duì)于 STORM)和可光切換熒光蛋白(對(duì)于 PALM)。dSTORM 或無(wú)激活劑 STORM方法允許使用與二抗偶聯(lián)的市售光可切換染料,而無(wú)需激活劑-報(bào)告劑對(duì)染料,這有利于多色分析。三色 STORM 分析通過(guò)將 STORM 與光譜分離(光譜解混)方法相結(jié)合,來(lái)解析具有重疊發(fā)射光譜的熒光團(tuán)。
3、成像速度和實(shí)時(shí)成像
商用 SIM 顯微鏡的時(shí)間分辨率與 STED 顯微鏡相似,優(yōu)于 STORM,因?yàn)?SIM 重建超分辨率圖像所需的原始顯微照片數(shù)量?jī)H為 9 到 15 張,而 STORM 則需要數(shù)萬(wàn)張。此外,與 STED 和 STORM 相比,SIM 需要較低的成像光強(qiáng)度。SIM 實(shí)時(shí)成像目前用于分析各種神經(jīng)系統(tǒng)結(jié)構(gòu),包括培養(yǎng)神經(jīng)元的生長(zhǎng)錐、生長(zhǎng)錐細(xì)胞骨架和囊泡、培養(yǎng)的海馬神經(jīng)元的樹(shù)突棘,以及大腦中的樹(shù)突和樹(shù)突棘,活斑馬魚(yú)幼蟲(chóng)或活老鼠。
STED 顯微鏡類(lèi)似于共聚焦顯微鏡,兩者都是掃描顯微鏡。點(diǎn)掃描顯微鏡允許對(duì)較小的區(qū)域或線(xiàn)進(jìn)行成像,以提高時(shí)間分辨率,而不是掃描整個(gè)視野。STED顯微鏡實(shí)現(xiàn)了視頻速率的快速實(shí)時(shí)成像;例如38.5 FPS用于分析囊泡融合和內(nèi)吞作用,28 FPS用于分析神經(jīng)元中的突觸蛋白 。
STORM (PALM, SMLM) 成像速度約為 0.1 FPS,因?yàn)樾枰獢?shù)萬(wàn)幀(顯微照片)來(lái)重建超分辨率圖像,比 SIM 和 STED 的時(shí)間分辨率低。目前,已經(jīng)開(kāi)發(fā)了多種算法來(lái)提高STORM的時(shí)間分辨率,包括識(shí)別可能具有重疊點(diǎn)擴(kuò)散函數(shù)的分子位置的多發(fā)射體擬合算法。STORM 已與 TIRF 顯微鏡相結(jié)合,因此具有低于 1 微米的淺成像深度,使用 STORM 可以對(duì)幾微米到 30 微米厚的切片進(jìn)行成像。
目前各種超分辨率顯微技術(shù)基本都可以實(shí)現(xiàn)商用,但是每種技術(shù)都有優(yōu)缺點(diǎn),在選擇用于項(xiàng)目的方法之前,需要綜合考慮。例如,如果項(xiàng)目需要最高分辨率,STORM 和 STED 可以提供目前商用超分辨率顯微鏡(橫向分辨率為 20 至 30 nm)的最佳分辨率。如果項(xiàng)目需要蛋白質(zhì)數(shù)量信息,STORM 已被證明可以提供定量信息。
二、超分辨率顯微鏡類(lèi)型對(duì)突觸分析的適用性
1、用于 NMJ 分析的 SIM
三維結(jié)構(gòu)照明顯微鏡 3D-SIM已用于分析大銜接蛋白 Ankyrin2-L通過(guò)調(diào)節(jié)突觸前微管和細(xì)胞粘附分子在穩(wěn)定果蠅幼蟲(chóng) NMJ 中的作用。3D-SIM 揭示了一個(gè)重復(fù)的晶格結(jié)構(gòu),其周期性約為 200 nm,由軸突中的 Ankyrin2-L 和 β-spectrin 組成,但在突觸前 boutons 中的組織結(jié)構(gòu)較差。
通過(guò)在小鼠 NMJ 中使用 3D-SIM,分析突觸蛋白的分布模式,包括突觸前活性區(qū)蛋白 Piccolo 和突觸后蛋白 rapsyn、電壓門(mén)控鈉通道和整合素 α7,相對(duì)于突觸后連接折疊的分布模式進(jìn)行了分析。與之前的報(bào)道一致,這些蛋白質(zhì)是在 NMJ 的預(yù)期位置觀(guān)察到的。
2、用于 NMJ 分析的 STED 顯微鏡
超分辨率顯微鏡在 NMJ 分析中的首次應(yīng)用是使用 STED 顯微鏡對(duì)果蠅NMJ 的活動(dòng)區(qū)進(jìn)行成像。活動(dòng)區(qū)是突觸前膜上的突觸囊泡釋放位點(diǎn)。活動(dòng)區(qū)域在電子顯微鏡圖像中顯示為果蠅NMJ 中的 T 條或脊椎動(dòng)物 NMJ 中的小聚集體。先前通過(guò)共聚焦顯微鏡顯示該蛋白質(zhì)在運(yùn)動(dòng)神經(jīng)末梢以點(diǎn)狀分布,每個(gè)淚點(diǎn)內(nèi)沒(méi)有任何明顯結(jié)構(gòu)。STED 顯微鏡的亞衍射極限分辨率首次揭示了每個(gè)淚點(diǎn)內(nèi)的結(jié)構(gòu),并闡明了每個(gè)淚點(diǎn)中 Bruchpilot 蛋白的環(huán)狀模式。
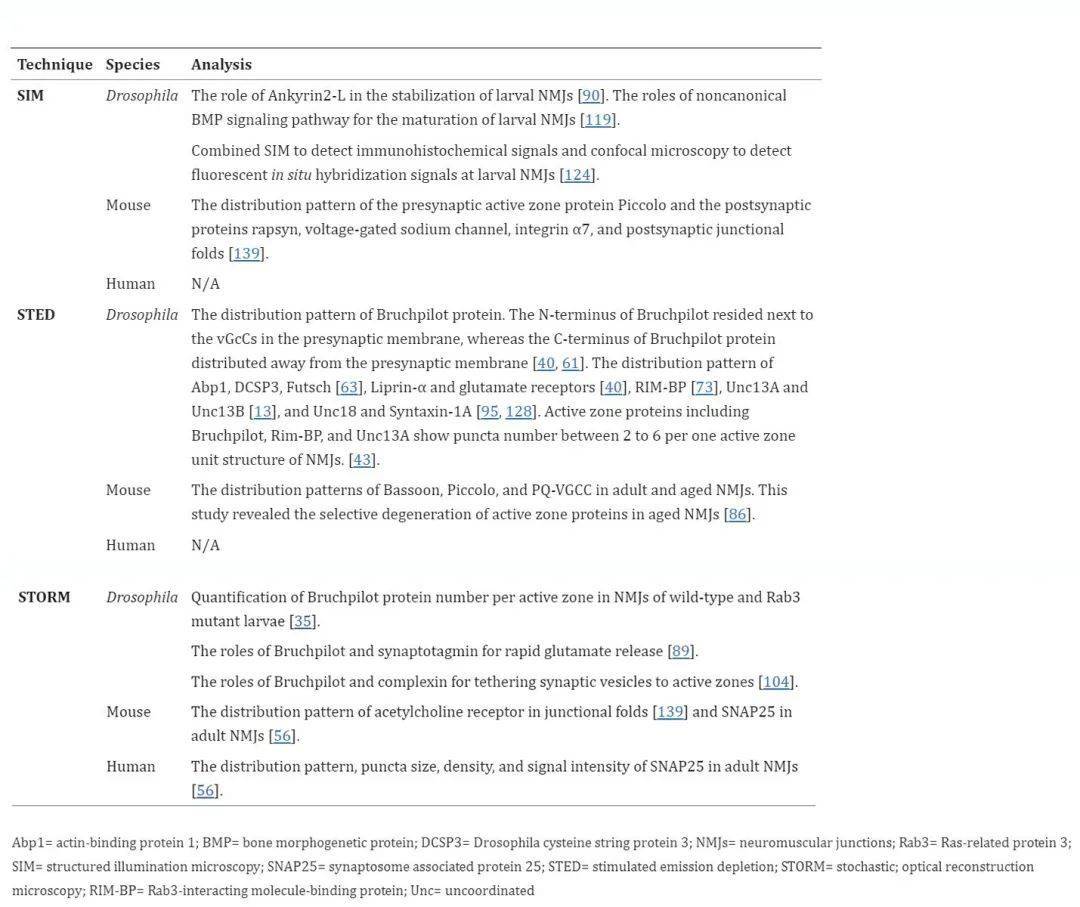
表2、用于 NMJ 分析的超分辨率顯微鏡技術(shù)
3、STORM 用于 NMJ 分析
與 STED 顯微鏡類(lèi)似,STORM 最初用于分析果蠅幼蟲(chóng) NMJ。使用直接隨機(jī)光學(xué)重建顯微鏡 (dSTORM) 定量分析果蠅幼蟲(chóng) NMJ 的活動(dòng)區(qū)。作為單分子定位顯微鏡方法,dSTORM 用于定量?jī)?nèi)源性蛋白質(zhì)。活性區(qū)特異性 Bruchpilot 蛋白的數(shù)量估計(jì)為每個(gè)活性區(qū) 137 個(gè)蛋白質(zhì),這些蛋白質(zhì)的四分之三被組織成大約 15 個(gè)不同的位置,每個(gè)位置有 7 個(gè) Bruchpilot 蛋白。這種定量 dSTORM 技術(shù)成功地顯示了 Rab3 突變幼蟲(chóng) NMJ 中每個(gè)活性區(qū)的 Bruchpilot 蛋白數(shù)量增加了大約 60%。此外,STORM 被用來(lái)分析 Bruchpilot 和 synaptotagmin 在快速谷氨酸釋放中的作用以及 Bruchpilot 和絡(luò)合蛋白在將突觸囊泡束縛到果蠅的活躍區(qū)中的作用幼蟲(chóng) NMJ。
在小鼠 NMJs中,基于 STORM 圖像,作者提出了一種新的乙酰膽堿受體分布模式,其中受體濃度在交界褶口的肩部較高,但在脊部較低。這種分布模式與經(jīng)典理解略有不同,其中乙酰膽堿受體被認(rèn)為分布在交界褶皺脊的頂部和肩部,而不是褶皺的底部。
作者使用 STORM 比較了人和小鼠 NMJ 以分析突觸體相關(guān)蛋白 25 (SNAP25) 的分布模式。在小鼠 NMJs 中,SNAP25 以點(diǎn)狀方式分布,其密度(每 μm 2 15 )類(lèi)似于活性區(qū)蛋白 Bassoon 和 Piccolo 的點(diǎn)狀密度(每 μm 10 2)。有趣的是,與小鼠 NMJ 相比,人類(lèi) NMJ 在淚點(diǎn)大小、每個(gè) NMJ 區(qū)域的淚點(diǎn)密度和免疫組織化學(xué)的信號(hào)強(qiáng)度方面顯示出更大的 SNAP25 值。基于這些發(fā)現(xiàn),作者提出人類(lèi)和小鼠 NMJ 之間存在差異。
03研究結(jié)論
果蠅 NMJ 的超分辨率顯微鏡研究已經(jīng)取得了長(zhǎng)足的進(jìn)步,并揭示了令人印象深刻的納米結(jié)構(gòu)和以前在電子顯微照片中被稱(chēng)為 T 型條的活性區(qū)的分子特性。良好的分子標(biāo)記(例如,活躍區(qū)的 Bruchpilot)和豐富的遺傳突變資源的結(jié)合為使用超分辨率顯微鏡研究果蠅 NMJ 生理修飾的分子機(jī)制提供了豐富的機(jī)會(huì)。哺乳動(dòng)物 NMJ 的超分辨率顯微鏡研究仍處于起步階段。據(jù)我們所知,這些超分辨率方法尚未用于脊椎動(dòng)物 NMJ 的實(shí)時(shí)成像。然而,已經(jīng)使用電子顯微鏡斷層掃描在青蛙和小鼠中研究了脊椎動(dòng)物 NMJ,揭示了突觸前活動(dòng)區(qū)的超微結(jié)構(gòu)細(xì)節(jié)。超分辨率顯微鏡提供了揭示這些建模結(jié)構(gòu)的分子身份的機(jī)會(huì),以便更好地了解脊椎動(dòng)物突觸,超分辨率顯微鏡的發(fā)展提高了對(duì)支撐分子機(jī)制的理解。
04超高分辨率顯微成像系統(tǒng)iSTORM
前文中提及的隨機(jī)光學(xué)重構(gòu)顯微鏡(STORM)技術(shù),目前已成功實(shí)現(xiàn)商用。 超高分辨率顯微成像系統(tǒng) iSTORM,成功實(shí)現(xiàn)了光學(xué)顯微鏡對(duì)衍射極限的突破,使得在 20 nm的分辨率尺度上從事生物大分子的單分子定位與計(jì)數(shù)、亞細(xì)胞及超分子結(jié)構(gòu)解析、生物大分子生物動(dòng)力學(xué)等的研究成為現(xiàn)實(shí),從而給生命科學(xué)、醫(yī)學(xué)等領(lǐng)域帶來(lái)重大性突破 。

圖2、超高分辨率顯微成像系統(tǒng)iSTORM。
超高分辨率顯微成像系統(tǒng) iSTORM 具有 20 nm超高分辨率、3通道同時(shí)成像、3D同步拍攝、實(shí)時(shí)重構(gòu)、2小時(shí)新手掌握等特點(diǎn),已實(shí)現(xiàn)活細(xì)胞單分子定位與計(jì)數(shù),并提供熒光染料選擇、樣本制備、成像服務(wù)與實(shí)驗(yàn)方案整體解決方案, 以納米級(jí)觀(guān)測(cè)精度、高穩(wěn)定性、廣泛環(huán)境適用、快速成像、簡(jiǎn)易操作等優(yōu)異特性,獲得了超過(guò)50家科研小組和100多位科研人員的高度認(rèn)可。
參考文獻(xiàn):
Badawi Y, Nishimune H. Super-resolution microscopy for analyzing neuromuscular junctions and synapses. Neurosci Lett. 2020 Jan 10;715:134644. doi: 10.1016/j.neulet.2019.134644. Epub 2019 Nov 22. PMID: 31765730; PMCID: PMC6937598.



