
慢性腎臟疾病影響著世界上10%以上的人口,其中大多數源于腎小球的損傷。腎小球過濾屏障(GFB)是一種能夠在血流和尿液之間選擇性滲透的復雜結構。 作為GFB組成部分之一的腎小球基底膜(GBM),是腎小球超濾的重要介質,它由內皮細胞和其兩側足細胞分泌的細胞外基質(ECM)蛋白組成。 一旦GFB中的任何組成部分出現損傷或遺傳缺陷都將會導致腎小球過濾屏障功能障礙,從而使得尿液中蛋白質含量升高引發腎臟疾病。
01研究介紹
Suleiman等人通過結合來自亞衍射分辨率隨機光學重建顯微鏡(STORM)和電子顯微鏡(EM)的數據,表明小鼠和人的腎小球基底膜中蛋白質排列相似,形成了獨特的分層結構,這表明基底膜組織在腎功能中起著關鍵作用。
同時,該研究揭示了細胞外基質蛋白的超微結構,通過對小鼠和人GBM中聚集蛋白、層粘連蛋白和膠原蛋白IV的N-末端和C-末端附近結構域的單獨分析,揭示了高度定向的大分子組織。除此之外,這項工作還提供了一種研究不同類型組織中基底膜結構的方法,首次實現了對復雜ECM組織的納米級觀測。
02研究結果
1、用STORM和STORM/Deep-Etch電子顯微鏡對比成像腎小球濾過屏障的超微結構
為了揭示 GBM 內的超分子結構,作者使用與 Alexa 647(一種明亮的熒光光敏染料)結合的抗體對腎臟切片中的腎小球進行了 STORM 成像。
由于 GBM 內致密的蛋白質網絡產生了強烈的熒光背景和光散射,對從腎臟切片獲取高分辨率 STORM 數據構成障礙,作者對固定和組織切片方法進行了改進,并最終確定在 200 納米(nm)厚度下對 Tokuyasu 冷凍包埋和冷凍切片最佳。
為了研究集聚蛋白(GBM的主要HSPG成分)在GBM中的組織,作者首先用抗集聚蛋白 C 的抗體標記腎切片,與傳統的 agrin 免疫熒光圖像相比,STORM 在 GBM 中解析了兩個不同的 agrinC 層(圖1-A,圖1-B)。
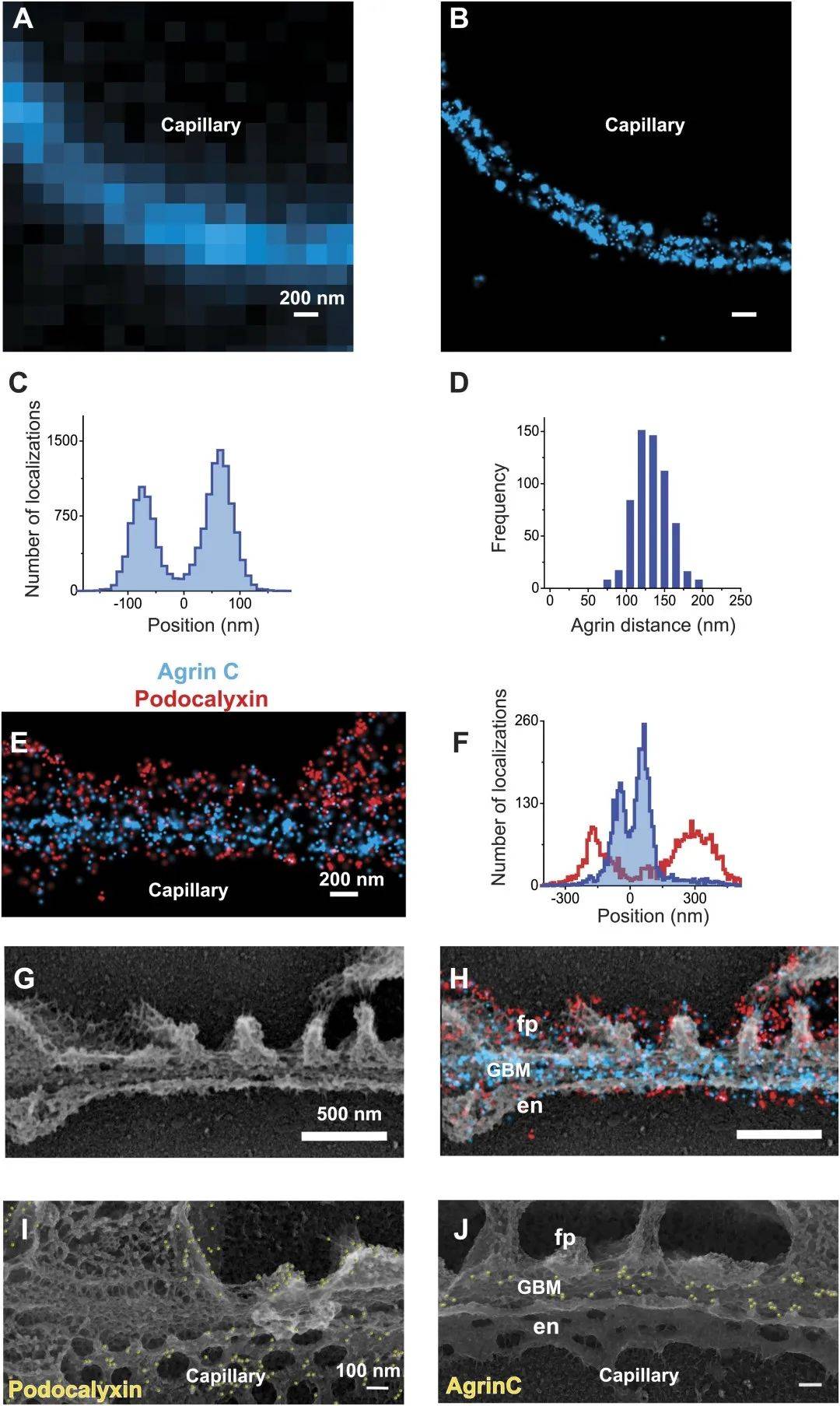
圖1、鼠GBM的STORM和STORM-EM圖像相關性
為了定量記錄 agrinC(集聚蛋白的 C 端 )的分布,作者數字化選擇了腎小球的多個區域。通過抗 agrinC 和唾液蛋白 podocalyxin 的抗體進行雙重標記,對 GBM 與側翼足細胞和內皮細胞之間的關系進行成像,后者在內皮細胞和足細胞表面都有表達。雙通道 STORM 成像顯示,兩層 agrinC 確實位于兩層 podocalyxin 之間(圖1-E、圖1-F和圖1-圖補充 1)。
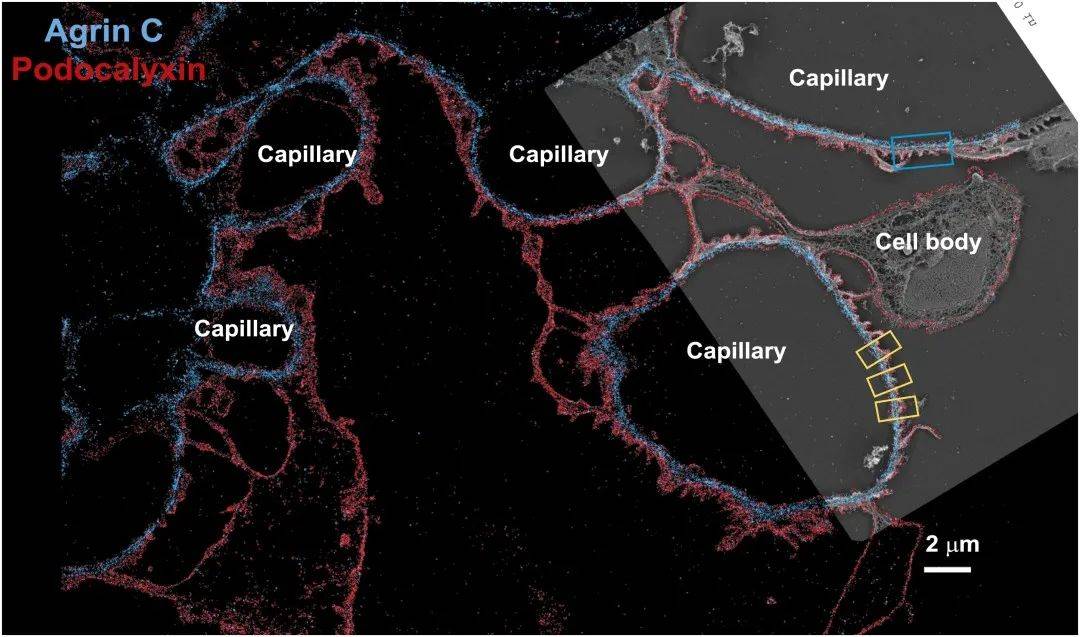
圖1-圖補充1、EM/STORM相關的低放大倍率圖像
為了進一步關聯 STORM 分子定位,作者開發了一種混合 STORM-電子顯微鏡 (EM) 方法(參見圖1-圖補充2中的示意圖),同樣也證實了 GFB 的超微結構特征。
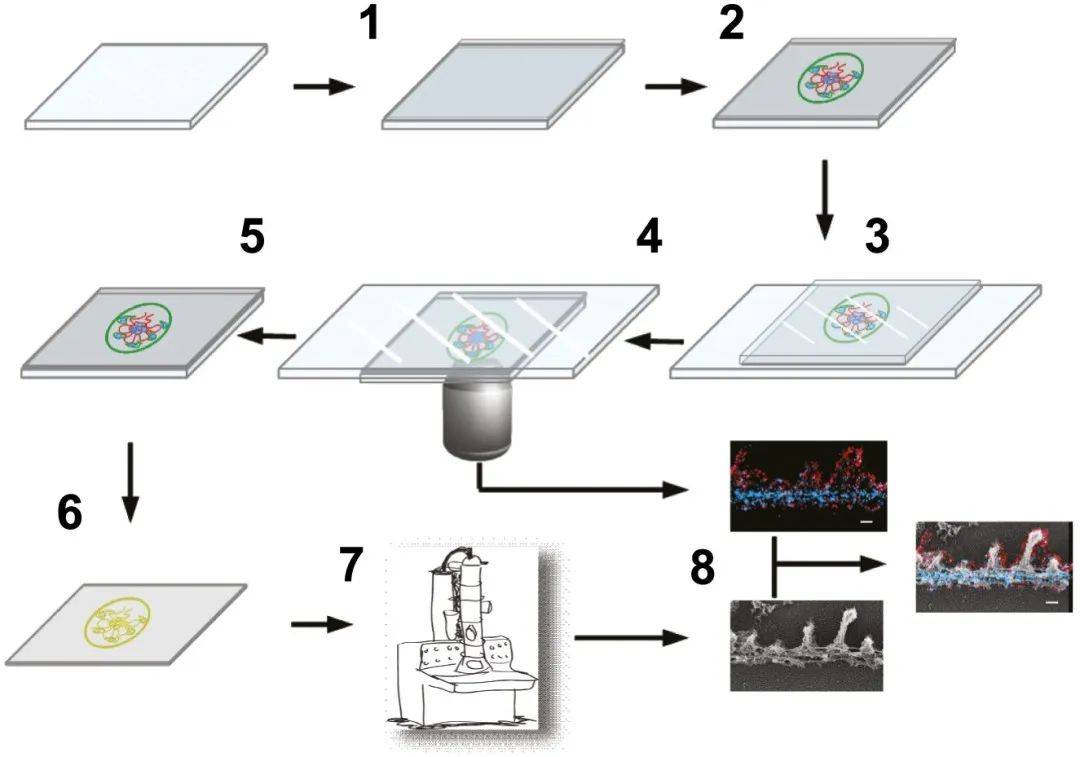
圖1-圖補充2、示意圖顯示處理樣品的步驟
2、在 GBM 內定位分子
在建立了樣本制備、STORM 成像和 EM 相關性的方法后,通過比較各種 ECM 組件的位置來分析 GBM 的分子組織。利用 agrinC 的穩健和雙峰分布,作者使用了一種定位方案,其中兩個 agrinC 層之間的中心位置被設置為原點,第二個蛋白質的位置,與 agrinC 一起通過雙色 STORM 成像,通過在多個區域和腎小球上重復該過程,可以高精度地確定 GBM 中各種蛋白質表位的位置。本研究中繪制的各種 ECM 蛋白及其表位如圖2-圖補充1所示。
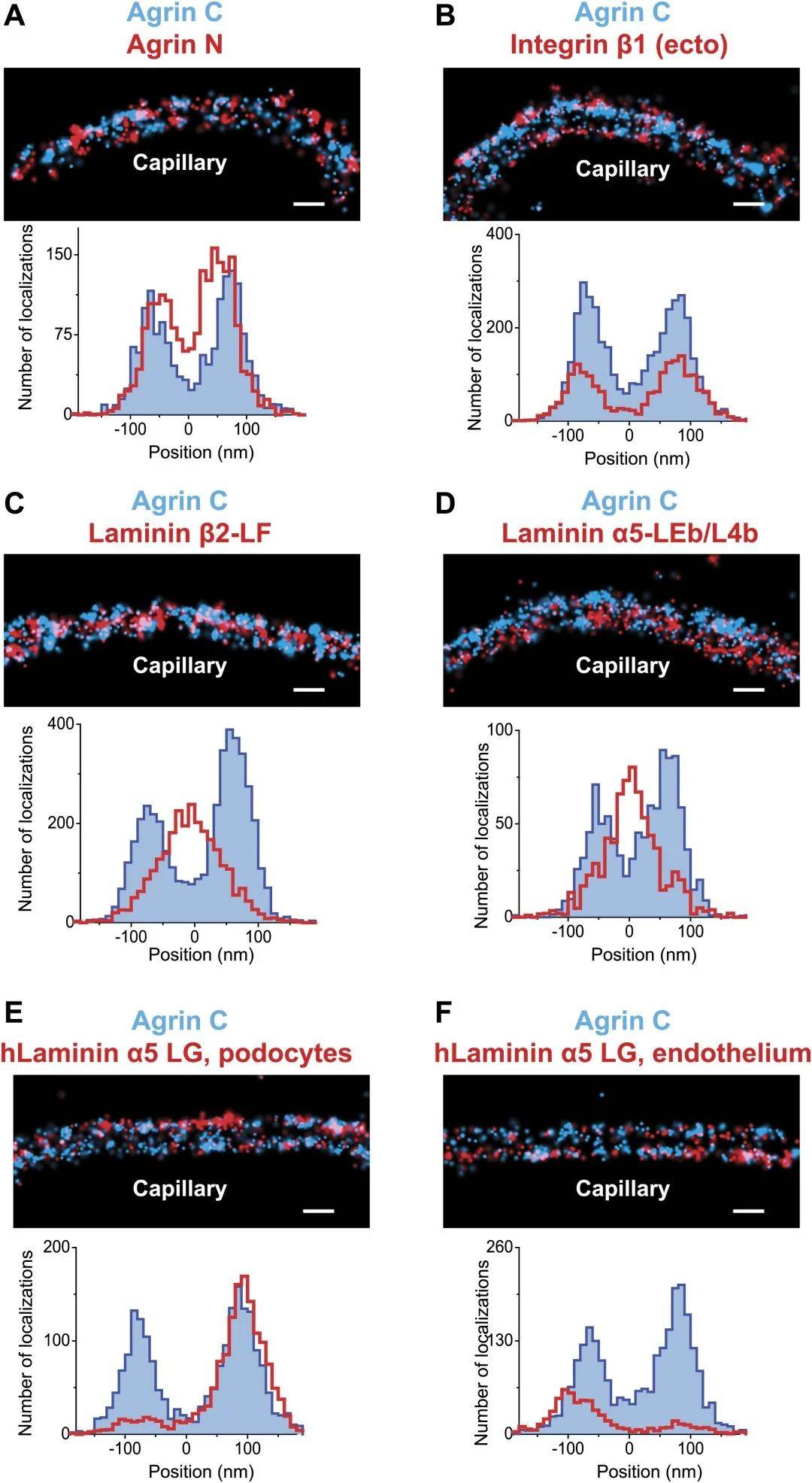
圖2、在GBM內定位分子結構域
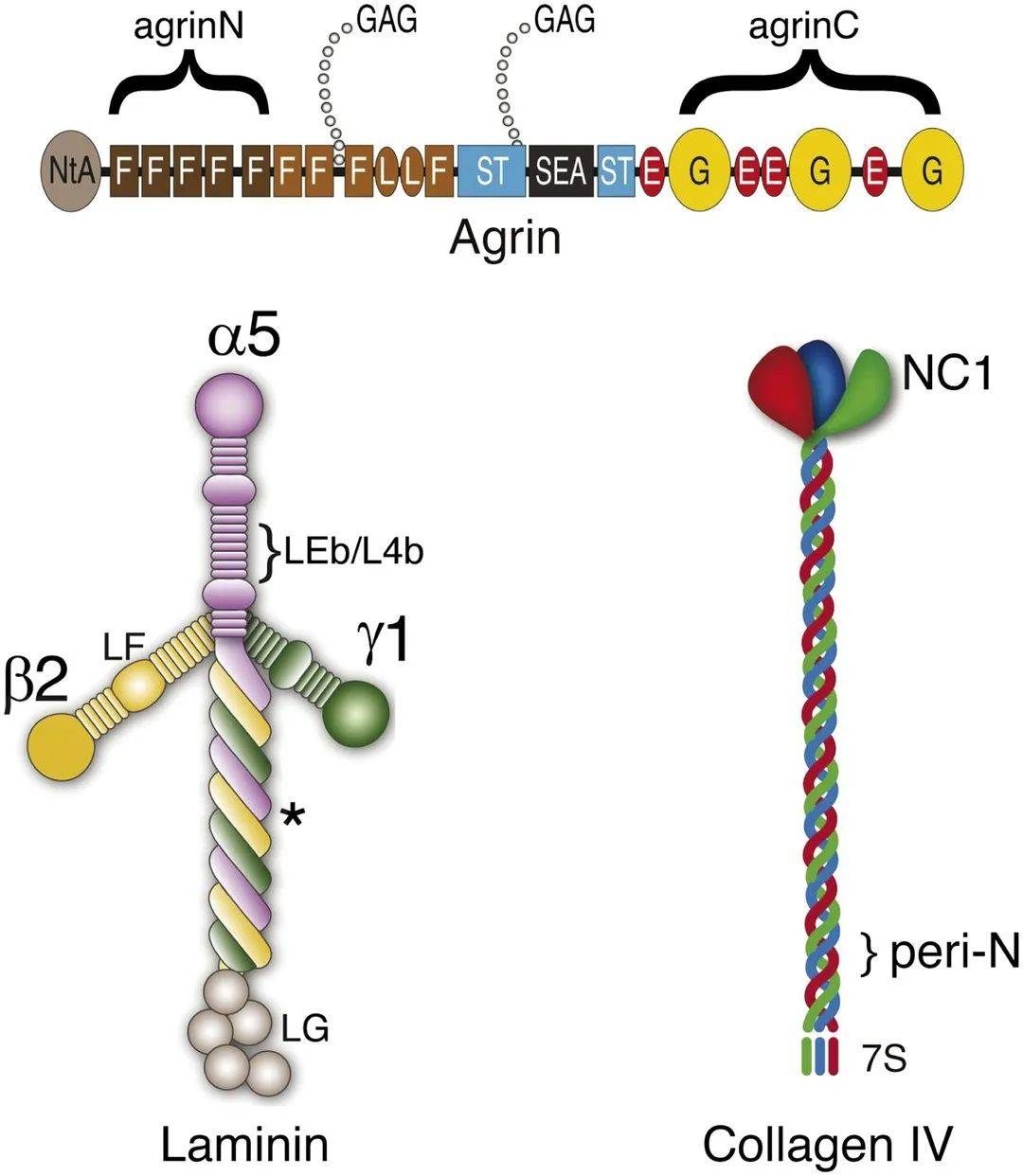
圖 2-圖補充1、抗原表位與Agrin、Laminin和Collagen IV結構之間的關系
3、腎小球基底膜成分在Alport綜合征小鼠模型中的分布
腎小球基底膜(GBM)成分的獨特分布促使作者評估 GBM 的組織是否在基底膜的特定疾病中受到破壞。因此,作者分析了常染色體隱性遺傳 Alport 綜合征的小鼠模型,該模型由于 COL4A3 無效突變而缺乏膠原α3α4α5(IV)網絡。
在人類和小鼠中,該網絡的缺乏會導致膠原 α1α1α2(IV)表達的代償性增加,通常會在成人 GBM 中以低水平被發現。盡管有這種代償作用,GBM 仍會出現節段性分裂和增厚,這與血尿、蛋白尿和進行性腎功能衰竭有關。
為了研究該疾病模型中 GBM 的結構,作者檢測了 agrinC 和膠原α1α1α2(IV)的組織,最終得出結論,完整的膠原 α3α4α5(IV)網絡有助于維持健康 GBM 中聚集蛋白和膠原 α1α1α2(IV)的組織。(圖3)
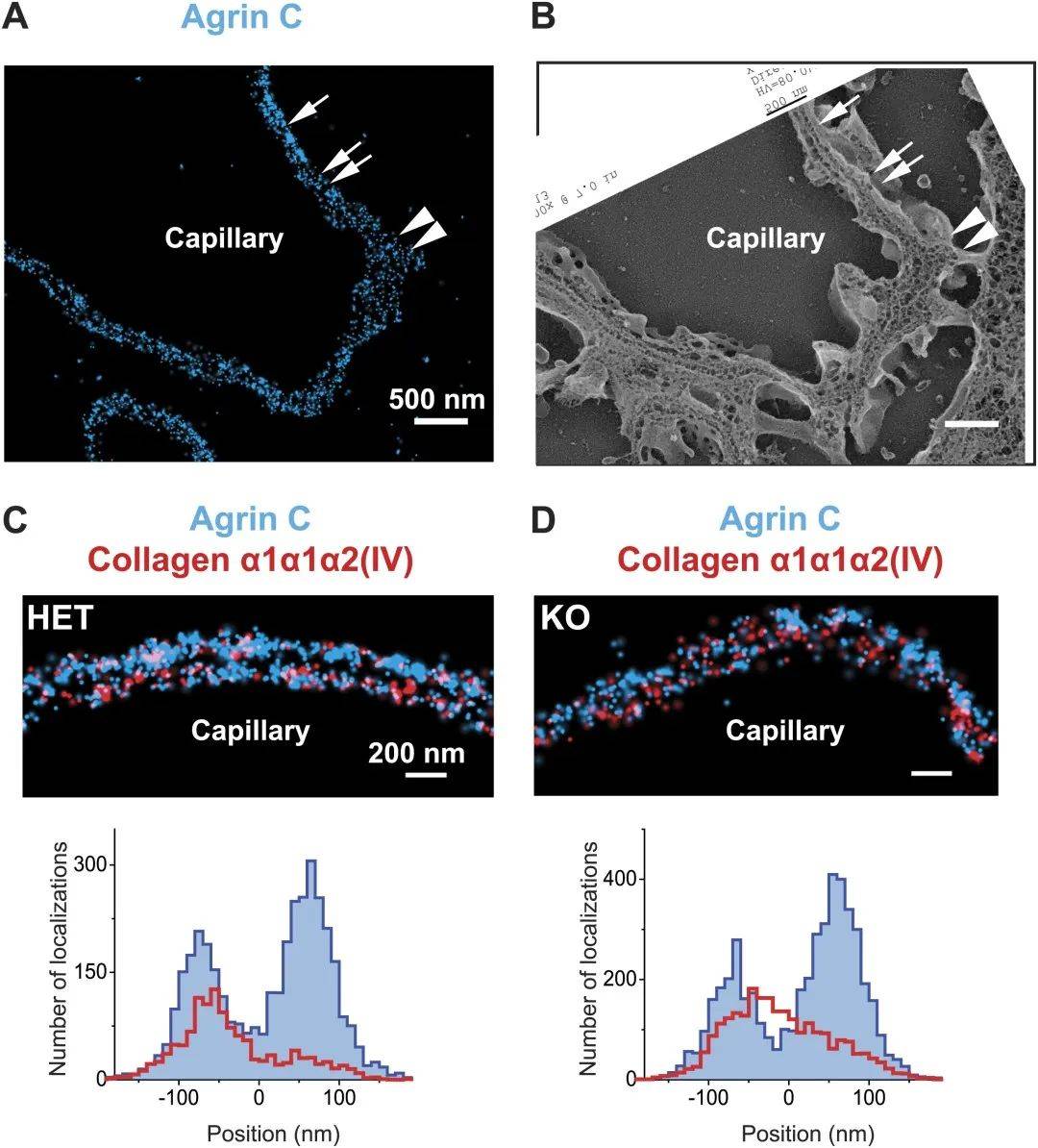
圖3、Alport綜合征小鼠模型中GBM分子結構的分解
03研究總結
確定細胞外基質蛋白(ECM)的結構、分子相互作用以及空間組織是理解其在組織功能、形態發生和疾病中發揮作用的重要步驟。該研究描述了一種新的超分辨率熒光顯微鏡方法來重建 GBM 內 ECM 蛋白的分子結構,并且通過使用 STORM 和 EM 對同一樣品進行超微結構成像,實現了在致密組織切片中觀測系統的納米級分子映射。這種方法的穩健和相對快速的吞吐量使我們能夠重建小鼠和人類惡性膠質瘤(GBMs)的分子結構。

圖4、力顯智能自主研發的超高分辨率顯微成像系統iSTORM
寧波力顯智能科技有限公司(INVIEW)現已發布的超高分辨率顯微成像系統 iSTORM,采用了源自諾貝爾化學獎原理的 STORM 超高分辨率顯微成像技術, 實現了光學顯微鏡對衍射極限的突破,使得在 20 nm的分辨率尺度上從事生物大分子的單分子定位與計數、亞細胞及超分子結構解析、生物大分子生物動力學等的研究成為現實,從而給生命科學、醫學等領域帶來重要突破 。
超高分辨率顯微成像系統 iSTORM 具有 20 nm超高分辨率、3通道同時成像、3D同步拍攝、實時重構、2小時新手掌握等特點,已實現活細胞單分子定位與計數,并提供熒光染料選擇、樣本制備、成像服務與實驗方案整體解決方案, 以納米級觀測精度、高穩定性、廣泛環境適用、快速成像、簡易操作等優異特 性,獲得了超過50家科研小組和100多位科研人員的高度認可。
有需要使用 STORM 成像技術來進行細胞研究的學者老師們,文末填寫問卷,即可有機會獲得 iSTORM 超高分辨率顯微成像系統試拍服務哦~
參考文獻:
Hani Suleiman, Lei Zhang, Robyn Roth, John E Heuser, Jeffrey H Miner, Andrey S Shaw, Adish Dani (2013) Nanoscale protein architecture of the kidney glomerular basement membrane eLife 2:e01149
關于我們:
寧波力顯智能科技有限公司(INVIEW)是專業從事超高分辨率顯微技術和產品研發的科技企業,依托復旦大學的自動控制、新一代信息技術及香港科技大學的生物、光學、圖像處理等的技術,擁有光學、生物、自控、機械、信息技術等多領域交叉學科技術團隊,將2014年諾貝爾化學獎技術產業化,推出了超高分辨率顯微成像系統iSTORM、細胞智能監控助手Cellaview等一系列產品,幫助人們以前所未有的視角觀察微觀世界,突破極限,見所未見。



