

01摘要
隨著技術(shù)的進(jìn)步,遠(yuǎn)場熒光顯微技術(shù)在圖像分辨率中取得了重大進(jìn)展,在兩個橫向維度上實現(xiàn)了20- 30nm的近分子分辨率。然而,三維(3D)納米分辨率成像仍然是一個挑戰(zhàn)。 在這里,作者通過使用光學(xué)散光以納米精度確定單個熒光團(tuán)的軸向和橫向位置來演示3D隨機(jī)光學(xué)重構(gòu)顯微鏡 (STORM)。光可切換探針的迭代、隨機(jī)激活可實現(xiàn)每個探針的高精度3D定位,因此無需掃描樣本即可構(gòu)建3D圖像。使用這種方法,作者在橫向尺寸上實現(xiàn)了20-30 nm的圖像分辨率,在軸向尺寸上實現(xiàn)了 50-60 nm的圖像分辨率。這一發(fā)展使我們能夠分辨納米級細(xì)胞結(jié)構(gòu)的 3D 形態(tài)。
02研究介紹(節(jié)選)
由于其非侵入性和多色能力,遠(yuǎn)場光學(xué)顯微鏡在結(jié)合熒光標(biāo)記時可提供具有最小擾動和生物分子特異性的生物樣本的三維 (3D) 成像。這些優(yōu)點使熒光顯微鏡成為生物學(xué)中使用最廣泛的成像方法之一。然而,衍射屏障將傳統(tǒng)光學(xué)顯微鏡的成像分辨率限制在橫向維度上的 200-300 nm,使許多細(xì)胞內(nèi)細(xì)胞器和分子結(jié)構(gòu)無法分辨。 最近,衍射極限已被超越,20 - 50 nm 的橫向成像分辨率已通過幾種“超分辨率”遠(yuǎn)場顯微鏡技術(shù)實現(xiàn),包括受激發(fā)射耗盡 (STED) 及其相關(guān)的 RESOLFT 顯微鏡、飽和結(jié)構(gòu)照明顯微鏡 (SSIM)、STORM、光激活定位顯微鏡 (PALM)和其他使用類似原理的方法。
雖然這些技術(shù)提高了 2D 圖像分辨率,但解析大多數(shù)細(xì)胞器和細(xì)胞結(jié)構(gòu)需要在三個維度上進(jìn)行高分辨率成像。三維熒光成像最常使用共焦或多光子顯微鏡進(jìn)行,其軸向分辨率通常在 500-800 nm 的范圍內(nèi),比橫向分辨率差兩到三倍。軸向成像分辨率可以通過 4Pi 和 I5M 顯微鏡提高到大約 100 nm 。此外,通過使用 4Pi 照明幾何沿軸向方向采用STED成像可以使軸向分辨率高達(dá) 30 - 50 nm,但相同的方案在橫向分辨率中并不能實現(xiàn)。
在這里,作者向我們展示了 3D STORM 成像,其空間分辨率比所有三個維度的衍射極限好10倍,且無需調(diào)試樣品或光束掃描。STORM 和 PALM 依賴于單分子檢測,并利用某些熒光團(tuán)的光可切換特性在時間上分離大量分子的其他空間重疊圖像,從而實現(xiàn)單個分子的高精度定位。除了檢測到的光子數(shù)量受到限制,單個熒光染料的橫向尺寸可以實現(xiàn)高達(dá) 1 nm 的定位精度。在這項工作中,作者使用散光成像方法來實現(xiàn) 3D STORM 成像。在 3D STORM 分析中,然后通過將其圖像的測量 wx 和 wy 值與校準(zhǔn)曲線進(jìn)行比較來確定每個光激活熒光團(tuán)的 z 坐標(biāo)。此外,對于浸入玻璃基板上的水溶液中的樣品,所有 z 定位都重新調(diào)整了 0.79 倍,以說明玻璃和水之間的折射率不匹配。
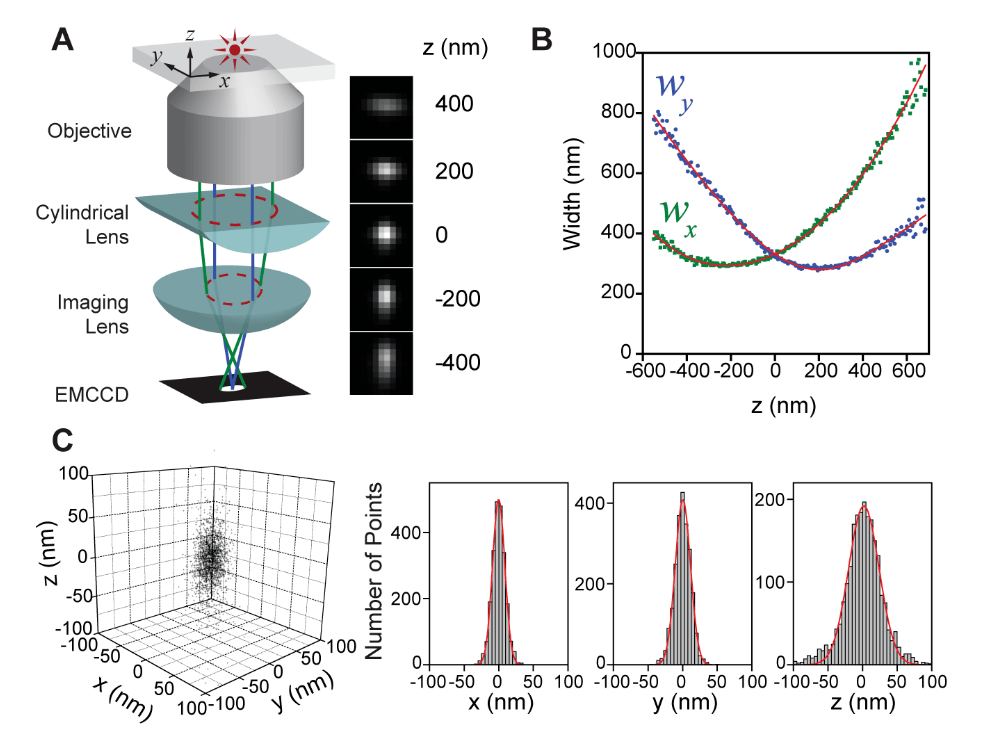
圖 1、3D STORM 方案。(A) 單個熒光團(tuán)的三維定位。(B) 作為從單個 Alexa 647 分子獲得的 z 函數(shù)的圖像寬度 wx 和 wy 的校準(zhǔn)曲線。(C) 單分子的三維定位分布。
STORM 的 3D 分辨率受限于單個光激活熒光團(tuán)在切換周期期間在三個維度上定位的精度。在這里,作者使用 Cy3 和 Alexa 647 作為激活劑和報告基因?qū)韴?zhí)行 3D STORM 成像。紅色激光 (657 nm) 用于對 Alexa 647 分子進(jìn)行成像并將其停用至黑暗狀態(tài),而綠色激光 (532 nm) 用于重新激活熒光團(tuán)。在發(fā)生永久性光漂白之前,每個激活子-報告子對可以循環(huán)打開和關(guān)閉數(shù)百次,使用物鏡型全內(nèi)反射熒光 (TIRF) 或落射熒光成像幾何,在每個開關(guān)循環(huán)平均可以檢測到 6000 個光子。這種可逆的開關(guān)行為提供了一種內(nèi)部控制來測量定位準(zhǔn)確性。
作為 3D STORM 的初始測試,作者將 200 nm 生物素化聚苯乙烯微球固定在玻璃表面上制備的模型樣品進(jìn)行成像,然后將樣品與 Cy3-Alexa 647 標(biāo)記的鏈霉抗生物素蛋白一起孵育,再用光切換探針涂覆微球。通過迭代、隨機(jī)激活光學(xué)可分辨 Alexa 647 分子的稀疏子集,獲得珠子的 3D STORM 圖像,從而確定單個分子的 x、y 和 z 坐標(biāo)。在多個激活周期的過程中,許多熒光團(tuán)的位置被確定并用于構(gòu)建完整的 3D 圖像。當(dāng)沿三個方向觀察時,微球圖像的投影近似球形,由于每個熒光團(tuán)的圖像同時編碼其 x、y 和 z 坐標(biāo),與 2D STORM 成像相比,在 3D STORM 中定位每個分子所花的時間更短。
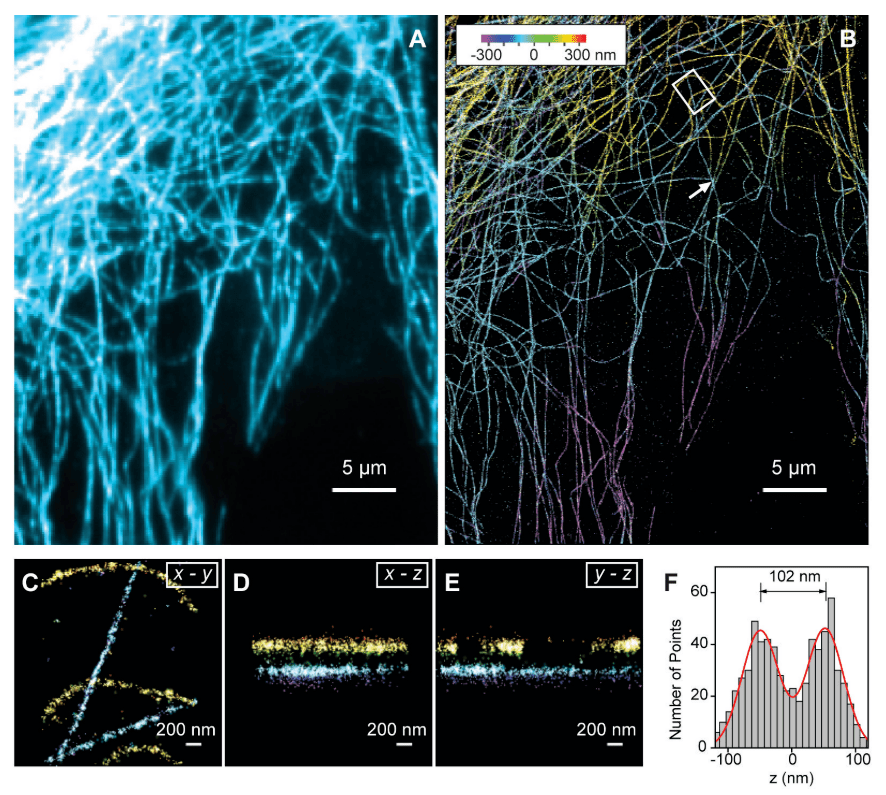
關(guān)于3D STORM應(yīng)用于細(xì)胞成像,作者對綠猴腎上皮 (BS-C-1) 細(xì)胞中的微管網(wǎng)絡(luò)進(jìn)行了間接免疫熒光成像。用一抗對細(xì)胞進(jìn)行免疫染色,然后用 Cy3 和 Alexa 647 雙標(biāo)記二抗。與傳統(tǒng)的寬視場熒光圖像(圖 2A、B)相比,3D STORM 圖像不僅顯示出分辨率的顯著提高,而且還提供了 z軸信息(圖 2B 中的顏色編碼)。從圖 2C-E中清晰可見在細(xì)胞的 x-y、x-z 和 y-z 橫截面中分布的多層微管絲。為了更定量地描述細(xì)胞成像分辨率,作者確定了細(xì)胞中的點狀物體,這些物體表現(xiàn)為遠(yuǎn)離任何可辨別的微管細(xì)絲的小簇定位,而這些簇可能代表非特異性附著在細(xì)胞上的單個抗體。
圖 2、細(xì)胞中微管的三維 STORM 成像。(A) BS-C-1 細(xì)胞大面積微管的常規(guī)間接免疫熒光圖像。(B) 同一區(qū)域的 3D STORM 圖像,z 位置信息根據(jù)彩色刻度條進(jìn)行顏色編碼。(C-E) (B) 中白框勾勒出的細(xì)胞小區(qū)域的 x-y、x-z 和 y-z 橫截面,顯示 5 個微管細(xì)絲。(F) 兩個微管的 z 剖面在 x-y 投影中交叉,但在 z 中相隔 102 nm,與 (B) 中箭頭指示的區(qū)域分開。
最后,為了證明 3D STORM 可以用于解析細(xì)胞中納米級結(jié)構(gòu)的 3D 形態(tài),作者對 BS-C-1 細(xì)胞中的網(wǎng)格蛋白涂層凹坑 (CCP) 進(jìn)行了成像。CCP 是球形籠狀結(jié)構(gòu),大小約為150-200 nm,由網(wǎng)格蛋白和細(xì)胞膜細(xì)胞質(zhì)側(cè)的輔助因子組裝而成,以促進(jìn)內(nèi)吞作用。為了對 CCP 進(jìn)行成像,作者采用了直接免疫熒光方案,使用的是針對網(wǎng)格蛋白Cy3 和 Alexa 647 雙重標(biāo)記的一抗。當(dāng)通過常規(guī)熒光顯微鏡成像時,所有 CCP 都顯示為幾乎衍射極限的斑點,沒有可辨別的結(jié)構(gòu)(圖 3A)。在丟棄z維信息的 2D STORM 圖像中,可以清楚地看到 CCP的圓形(圖 3B、D)。從 180 ± 40 nm 的 2D 投影圖像測量的 CCP 的尺寸分布在數(shù)量上與使用電子顯微鏡確定的尺寸分布一致 (32)。包括 z 維度的信息使我們能夠清楚地看到凹坑的 3D 結(jié)構(gòu)(圖 3C,E - H)。圖 3C 和 3E 顯示了圖像的 x-y 橫截面,取自細(xì)胞表面凹坑開口附近的區(qū)域。凹坑外圍的圓形環(huán)狀結(jié)構(gòu)顯示出較高的分辨率。凹坑的連續(xù) x-y 和 x-z 橫截面(圖 3F-H)清楚地揭示了這些納米級結(jié)構(gòu)的三維半球籠狀形態(tài),這在 2D STORM 圖像中是無法觀察到的。總之,作者通過 STORM 顯微鏡展示了具有 20-30 nm 橫向分辨率和 50-60 nm 軸向分辨率的 3D 超分辨率成像。這種成像能力允許在環(huán)境條件下以光學(xué)方式解析細(xì)胞結(jié)構(gòu)的納米級特征,其分辨率以前只能用電子顯微鏡才能看到。
圖 3. 細(xì)胞中網(wǎng)格蛋白包被的凹坑的 3D STORM 成像。(A) BS-C-1 細(xì)胞區(qū)域中網(wǎng)格蛋白的常規(guī)直接免疫熒光圖像。(B) 同一區(qū)域的 2D STORM 圖像,包括不同 z 位置的所有定位。(C) 同一區(qū)域的 x-y 橫截面 (z 中厚 50 nm), 顯示質(zhì)膜處 CCP 外圍的環(huán)狀結(jié)構(gòu)。(D, E) 2D STORM (D) 中兩個附近 CCP 的放大圖及其 3D 圖像 (E) 中 100 nm 厚的 x-y 橫截面。(F - H) CCP 的串行 x-y 橫截面(z 方向每個 50 nm 厚)(F)和 x-z 橫截面(y 方向每個 50 nm 厚)(G),以及 x-y 和 x-z 橫截面3D 透視圖 (H),顯示坑的籠狀結(jié)構(gòu)。
03超高分辨率顯微成像系統(tǒng)iSTORM
寧波力顯智能科技有限公司(INVIEW)現(xiàn)已發(fā)布的超高分辨率顯微成像系統(tǒng) iSTORM,采用了源自諾貝爾化學(xué)獎原理的 STORM 超高分辨率顯微成像技術(shù), 實現(xiàn)了光學(xué)顯微鏡對衍射極限的突破,使得在 20 nm的分辨率尺度上從事生物大分子的單分子定位與計數(shù)、亞細(xì)胞及超分子結(jié)構(gòu)解析、生物大分子生物動力學(xué)等的研究成為現(xiàn)實,從而給生命科學(xué)、醫(yī)學(xué)等領(lǐng)域帶來重大突破 。

圖4、力顯智能自主研發(fā)的超高分辨率顯微成像系統(tǒng)iSTORM
超高分辨率顯微成像系統(tǒng) iSTORM 具有 20 nm超高分辨率、3通道同時成像、3D同步拍攝、實時重構(gòu)、2小時新手掌握等特點,已實現(xiàn)活細(xì)胞單分子定位與計數(shù),并提供熒光染料選擇、樣本制備、成像服務(wù)與實驗方案整體解決方案, 以納米級觀測精度、高穩(wěn)定性、廣泛環(huán)境適用、快速成像、簡易操作等優(yōu)異特性,獲得了超過50家科研小組和100多位科研人員的高度認(rèn)可。
有需要使用 STORM 成像技術(shù)來進(jìn)行細(xì)胞研究的學(xué)者老師們,文末填寫問卷,即可有機(jī)會獲得 iSTORM 超高分辨率顯微成像系統(tǒng)試拍服務(wù)哦~
參考文獻(xiàn):
Huang B, Wang W, Bates M, Zhuang X. Three-dimensional super-resolution imaging by stochastic optical reconstruction microscopy. Science. 2008 Feb 8;319(5864):810-3. doi: 10.1126/science.1153529. Epub 2008 Jan 3. PMID: 18174397; PMCID: PMC2633023.
關(guān)于我們:
寧波力顯智能科技有限公司(INVIEW)是專業(yè)從事超高分辨率顯微技術(shù)和產(chǎn)品研發(fā)的科技企業(yè),依托復(fù)旦大學(xué)的自動控制、新一代信息技術(shù)及香港科技大學(xué)的生物、光學(xué)、圖像處理等的技術(shù),擁有光學(xué)、生物、自控、機(jī)械、信息技術(shù)等多領(lǐng)域交叉學(xué)科技術(shù)團(tuán)隊,將2014年諾貝爾化學(xué)獎技術(shù)產(chǎn)業(yè)化,推出了超高分辨率顯微成像系統(tǒng)iSTORM、細(xì)胞智能監(jiān)控助手Cellaview等一系列產(chǎn)品,幫助人們以前所未有的視角觀察微觀世界,突破極限,見所未見。



